Cho m gam rắn A gồm CuO, Cu, Cu(NO3)2 phản ứng với dd HCl. Sau phản ứng thu được 17,92 lít khí G (đktc); biết tỷ khối hơi của G so với H2 bằng 22 và thu được dung dịch B chứa 202,5 gam một chất tan duy nhất. Giá trị m là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


QT cho electron:
Fe → Fe2+ + 2e
Mg → Mg2+ + 2e
QT nhận electron:
Ag+ + 1e → Ag
Cu2+ + 2e → Cu
Ta có: nAgNO3= 0,1 mol; nCu(NO3)2= 0,16 mol; nH2= 0,17 mol
Nhìn chung qua quá trình phản ứng thì 3 muối còn lại sẽ là: Cu(NO3)2dư, Fe(NO3)2; Mg(NO3)2 và các kim loại Mg, Fe đều phản ứng hết.
Sơ đồ phản ứng tiếp theo:
⎧⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎨⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎩Mg(NO3)2 xFe(NO3)2 yCu(NO3)2NaOH−−−→⎧⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎨⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎩Mg(OH)2Fe(OH)2Cu(OH)2O2,to−−−→⎧⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎨⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎩MgO x1/2Fe2O3 y/2CuO
Ta có các PT: nH2 = x + y = 0,17
mchất rắn = 40x + 80y + 80z = 10,4 g
Bảo toàn số mol nguyên tử N trong các muối:
nN-AgNO3 + nN-Cu(NO3)2 = nN-Fe(NO3)2 + nN-Mg(MO3)2
Þ 0,1.1 + (0,16 – z).2 = 2x + 2y
Từ đó giải ra x = 0,16; y = 0,01; z = 0,04
=> m = 0,16.24 + 0,01.56 = 4,4 gam.
Khối lượng các muối là: 23,68g; 1,8g; 7,52 g
Muối có phân tử khối lớn nhất trong B là Cu(NO3)2 0,04 mol có khối lượng là 7,52 gam

a) \(n_{Cu\left(NO_3\right)_2}=\dfrac{282}{188}=1,5\left(mol\right)\)
=> \(n_{Cu\left(NO_3\right)_2\left(pư\right)}=\dfrac{1,5.90}{100}=1,35\left(mol\right)\)
PTHH: 2Cu(NO3)2 --to--> 2CuO + 4NO2 + O2
______1,35------------>1,35------------->0,675
=> mCuO = 1,35.80 = 108(g)
=> VO2 = 0,675.22,4 = 15,12 (l)
b) Gọi số mol Cu(NO3)2 cần nung là a (mol)
=> \(n_{Cu\left(NO_3\right)_2\left(pư\right)}=\dfrac{90a}{100}=0,9a\left(mol\right)\)
PTHH: 2Cu(NO3)2 --to--> 2CuO + 4NO2 + O2
______0,9a---------------------->1,8a--->0,45a
=> (1,8a+0,45a).22,4 = 5
=> a = 0,0992 (mol)
=> \(m_{Cu\left(NO_3\right)_2}=0,0992.188=18,6496\left(g\right)\)

Đáp án A.
Vì phản ứng giữa Al và AgNO3 xảy ra trước nên kim loại sau phản ứng phải có Ag, kế đến là CuSO4 có phản ứng tạo thành Cu. Theo giả thiết, có ba kim loại → kim loại thứ ba là Fe còn dư.
Ta có: nFe = 2,8/5,6 = 0,05 (mol)
nAl = 0,81/27 = 0,03 (mol)
và = 0,672/22,4 = 0,03 (mol)
Phản ứng: Fedư + 2HCl → FeCl2 + H2
(mol) 0,03 0,03
→ Số mol Fe phản ứng với muối: 0,05 – 0,03 = 0,02 (mol)
2Al + 3Cu2+ → 2Al3+ + 3Cu
Fe + 2Ag+ → Fe2+ + 2Ag
Fe + Cu2+ → Fe2+ + Cu
Ta có sự trao đổi electron như sau:
Al → Al3+ + 3e Fe → Fe2+ + 2e
0,03 0,09 (mol) 0,02 0,04 (mol)
Ag+ + 1e → Ag Cu2+ + 2e → Cu
x x x (mol) y 2y y (mol)
→ x + 2y = 0,09 + 0,04 = 0,13 (1) ; 108x + 64y + 56.0,03 = 8,12 (2)
Giải hệ phương trình (1) và (2), ta được x = 0,03; y = 0,05.
Vậy:


\(n_{HCl}=\dfrac{58,4.15\%}{36,5}=0,24\left(mol\right)\\ Fe+2HCl\rightarrow\left(t^o\right)FeCl_2+H_2\\ n_{Fe}=n_{H_2}=\dfrac{0,24}{2}=0,12\left(mol\right)\\ \Rightarrow V1=V_{H_2\left(đktc\right)}=0,12.22,4=2,688\left(l\right)\\ x=m_{Cu}=m_{hhA}-m_{Fe}=15,68-0,12.56=8,96\left(g\right)\\ b,n_{Cu}=\dfrac{8,96}{64}=0,14\left(mol\right)\\ 2Fe+3Cl_2\rightarrow\left(t^o\right)2FeCl_3\\ Cu+Cl_2\rightarrow\left(t^o\right)CuCl_2\\ n_{Cl_2}=\dfrac{3}{2}.n_{Fe}+n_{Cu}=\dfrac{3}{2}.0,12+0,14=0,32\left(mol\right)\\ \Rightarrow V2=V_{Cl_2\left(đktc\right)}=0,32.22,4=7,168\left(l\right)\\ y=m_{muối}=m_{AlCl_3}+m_{CuCl_2}=0,12.133,5+0,14.135=34,92\left(g\right)\)
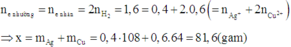

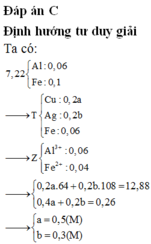

155,2
Cách giải chi tiết như thế nào vậy ?