1 nguyên tố X có thể tạo thành với Al hợp chất AlaXb ; một phân tử gồm 5 nguyên tử ,khối lượng của phân tử là150 đvC
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


vì nhôm (Al) hóa trị 3 nên hợp chất có dạng :\(Al_aX_3\) gồm 5 nguyên tử \(\Rightarrow a=5-3=2\) \(Al_2X_3\)
\(\Rightarrow\) X có hóa trị 2
\(M=27.2+X.3=150\)
\(\Rightarrow X=32\) => Lưu huỳnh ( S) thõa mãn hóa trị 2.
CTHH của hợp chất \(Al_2S_3\) ( nhóm sulfua ) .
công thức hh dạng: AlaXb mà 1 ptử của nó có 5 ngtử
ta có Al hóa trị 3 nên có tối đa 2 ngtử Al trong AlaXb
theo bài ra ta có: 27.2 + 3.X =150 => X = 32 = S(lưu huỳnh)
cthh là Al2S3

Trả lời
Ta thấy:
a + b = 5
Đặt trường hợp thôi
1. Với a = 1 => b = 4 => Mx = 30.75
2. Với a = 2 => b = 3 => Mx = 32
3. Với a = 3 => b = 2 => Mx = 13.8
4. Với a = 4 => b = 1 => Mx = 42.
Trong 4 trường hợp thì trường hợp 2 có M = 32 là của Lưu huỳnh (S)
=> Hợp chất có công thức Al2S3.

Công thức hh dạng AlaXb mà 1 phân tử có 5 nguyên tử
Ta có:
Al hóa trị 3 nên tối đa 2 nguyên tử Al trong AlaXb
Theo đề bài ta có:
27 . 2 + 3 . x = 150
=> x = 32 = S(lưu huỳnh)
Cthh là Al2S3

Bài 1
Gọi CTHH của hợp chất là X2O5
Theo đề ra, ta có:
2X2X+16.5.100%=43,67%2X2X+16.5.100%=43,67%
Giải phương trình, ta được X = 31
=> X là P
=> CTHH của hợp chất: P2O5
xin lỗi tôi chỉ giúp được bạn bài 1
Bài 1:
\(\%_O=100\%-82,97\%=17,03\%\\ CTTQ:X_2O\\ \Rightarrow M_{X_2O}=\dfrac{16}{17,03\%}\approx 94(g/mol)\\ \Rightarrow M_X=\dfrac{94-16}{2}=39(g/mol)(K)\\ \Rightarrow CTHH:K_2O\)
bài 2:
\(CTTQ_Y:S_xO_y\\ \Rightarrow M_{S_xO_y}=\dfrac{16y}{50\%}=32y(g/mol)\\ \Rightarrow 32x+16y=32y\Rightarrow 32x=16y\\ \Rightarrow 2x=y\Rightarrow \dfrac{x}{y}=\dfrac{1}{2}\\ \Rightarrow x=1;y=2\\ \Rightarrow CTHH_Y:SO_2\)

Bài 1 :
$X(NO_3)_2$ suy ra X có hóa trị II
$YO$ suy ra Y có hóa trị II
Theo quy tắc hóa trị thì CTHH tạo bởi X và Y là XY

a)
$x = 2 ; y = 3$
PTHH : $2Al(OH)_3 + 3H_2SO_4 \to Al_2(SO_4)_3 + 6H_2O$
b)
Tỉ lệ số phân tử $Al(OH)_3$ : số phân tử $H_2SO_4$ là 2 : 3
c)
$\%Al = \dfrac{27}{78}.100\% =34,6\%$
d)
$n_{Al(OH)_3} = \dfrac{7,8}{78} = 0,1(mol)$
Theo PTHH : $n_{Al_2(SO_4)_3} = \dfrac{1}{2}n_{Al(OH)_3} = 0,05(mol)$
$m_{Al_2(SO_4)_3} = 0,05.342 = 17,1(gam)$
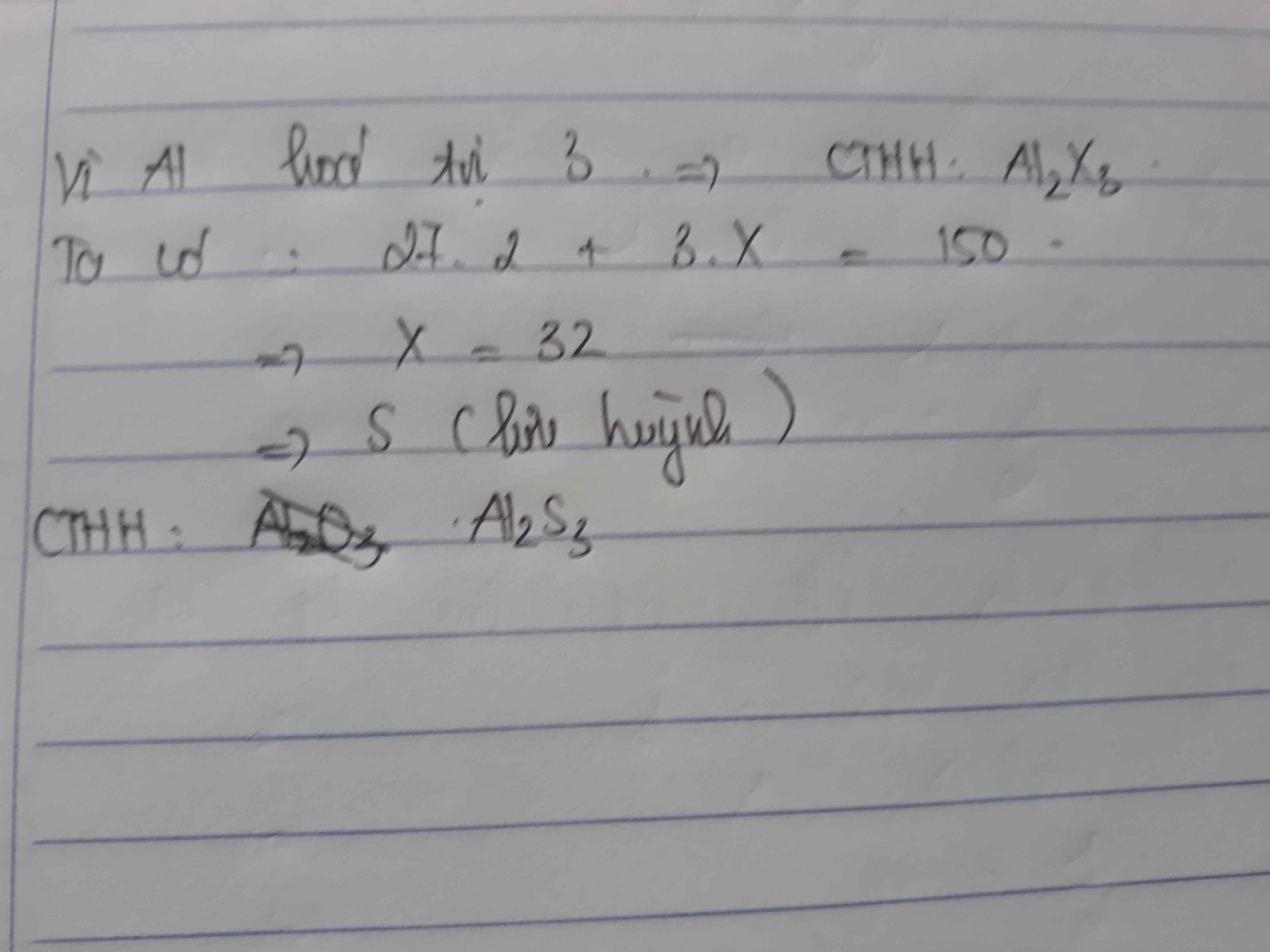
Al luôn hóa trị 3, các NTHH có hóa trị từ 1->7
+ TH1: X(I)=> có 4 nguyên tử (loại)
+TH2:X(II)=> có 5 nguyên tử(chọn)
+TH3:X(III)=>có 2 nguyên tử (loại)
+TH4:X(IV)=>có 7 nguyên tử(loại)
+TH5:X(V)=> có 8 nguyên tử (loại)
+TH6:X(VI)=> có 3 nguyên tử (loại)
+TH7LX(VII)=>có 10 nguyên tử(loại)
=> Al2X3
ta có:
150=2.27+3.X=54+3X
=>X=32=>X là S