tính khối lượng K2O và khối lượng dung dịch KOH 8% cần dùng để pha chế được 653g dung dịch KOH 28%
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) \(n_{K_2O}=\dfrac{37,6}{94}=0,4\left(mol\right)\)
PTHH: K2O + H2O --> 2KOH
0,4------------>0,8
=> mKOH = 0,8.56 = 44,8 (g)
b) \(C_M=\dfrac{0,8}{0,5}=1,6M\)
c)
PTHH: 4K + O2 --to--> 2K2O
0,2<----0,4
=> VO2 = 0,2.22,4 = 4,48 (l)

n(K2O)=0.5 mol
K2O + H2O --> 2KOH
--(0.5)-----------1 mol
=> mKOH= b= 56g
Gọi m là khối lượng ban đầu của dd KOH 8% ban đầu, sau khi cho K2O vào dd, thì K2O bị hòa tan hết tạo ra dd KOH 21% có khối lượng là m+47 (theo định luật bảo toàn khối lượng.
ta có phương trình sau:
0.08m+56=0.21(m+47)
igải phương trình trên ta có nghiệm m=354.846 (g)
Chọn A

- Khối lượng CuSO4 có trong 150 gam dung dịch CuSO4 20% là:
\(mCuSO_4=\dfrac{150.2}{100}=3\left(g\right)\)
Khi pha chế 150 gam dung dịch CuSO4 2% từ dung dịch CuSO4 20% thì khối lượng chất tan là CuSO4 không đổi vẫn là 3 gam
- Khối lượng dung dịch CuSO4 20% có chứa 3 gam CuSO4 là:
\(m_{dd}=\dfrac{3.100}{20}=15\left(g\right)\)
- Khối lượng nước cần dùng để pha chế là: 150-15=135 (gam)

a) \(2KOH+H_2SO_4\rightarrow K_2SO_4+2H_2O\)
\(n_{KOH}=\dfrac{200.11,2\%}{56}=0,4\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{1}{2}n_{KOH}=0,2\left(mol\right)\)
\(m_{ddH_2SO_4}=\dfrac{0,2.98}{10\%}=196\left(g\right)\)
b) \(n_{K_2SO_4}=\dfrac{1}{2}n_{KOH}=0,2\left(mol\right)\)
\(m_{ddsaupu}=200+196=396\left(g\right)\)
=> \(C\%_{K2SO4}=\dfrac{0,2.174}{396}.100=8,79\%\)
c) \(3KOH+FeCl_3\rightarrow Fe\left(OH\right)_3+3KCl\)
\(n_{FeCl_3}=n_{Fe\left(OH\right)_3}=\dfrac{1}{3}n_{KOH}=\dfrac{2}{15}\left(mol\right)\)
=>\(V_{FeCl_3}=\dfrac{2}{15}=0,13\left(l\right)\)
\(m_{Fe\left(OH\right)_3}=\dfrac{2}{15}.107=14,27\left(g\right)\)

\(n_{NaOH}=0,2.2,5=0,5\left(mol\right)\\ m_{NaOH}=0,5.40=20g\\ m_{\text{dd}}=\dfrac{100.20}{40}=50g\)

* Phần tính toán:
Khối lượng dung dịch NaOH: m d d = D.V = 1,1.2000=2200(g)
Khối lượng NaOH có trong 2 lit dung dịch:
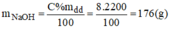
Gọi x(ml) là thể tích của dung dịch NaOH 3% ⇒ m d d = V.d = 1,05.x
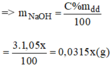
Gọi y(ml) là thể tích của dung dịch NaOH 10% ⇒ m d d = V.d = 1,12.y
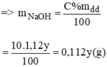
Ta có hệ phương trình sau: 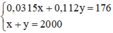
Giải hệ phương trình trên, ta được: 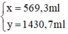
* Cách pha chế:
Đong lấy 569,3ml dung dịch NaOH 3% và 1430,7ml dung dịch NaOH 10% vào bình có dung dịch khoảng 3 lit. Trộn đều ta được 2 lit dung dịch NaOH 8% có khối lượng riêng 1,1g/ml.

m(đường)= 150 . 25%= 37,5(g)
=> m(H2O)=150 - 37,5=112,5(g)
=> Pha chế: Cho 37,5 gam đường vào 112,5 gam nước (112,5ml H2O). Khuấy đều ta được 150 gam dd đường 25%.
Coi K2O là dd có nồng độ là 100%
Gọi khối lượng K2O cần dùng m1 gam (m1>0)
Khối lượng dd KOH 8% cần dùng là m2 gam (m2>0)
Ta có quy tắc đường chéo:
=> \(\dfrac{m1}{m2}=\dfrac{20}{72}=\dfrac{5}{18}\)
=> 5m2= 18m1 <=> 5m2 - 18m1=0
T có hệ phương trình: \(\left\{{}\begin{matrix}5m_2-18m_1=0\\m_2+m_1=653\end{matrix}\right.\)
=> m1= 141,957 (g) ; m2= 511,043 (g)
Vậy cần 141,957 gam K2O và 511,043 gam dd KOH để pha chế được 652 gam dd KOH 28%
Sao bạn làm ra hay vậy?