Đốt cháy hoàn toàn 6,48 gam hỗn hợp chất rắn X gồm Cu, CuS, FeS, FeS2, FeCu2S2, S thì cần 2,52 lít O2 và thấy thoát ra 1,568 lít SO2. Mặt khác cho 6,48 gam X tác dụng với dung dịch HNO3 đặc nóng dư thu được V lít NO2 ( là sản phẩm khử duy nhất) và dung dịch A. Cho dung dịch A tác dụng Ba(OH)2 dư thu được m gam kết tủa. Biết thể tích các khí đều đo ở điều kiện tiêu chuẩn. Tính V và m
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Phương pháp:
Quy đổi hỗn hợp về Cu, Fe, O
Bảo toàn khối lượng
Bảo toàn electron
Hướng dẫn giải:
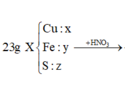
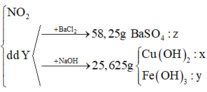
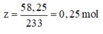
=> mCu + mFe = 23 – 0,25 . 32 = 15g
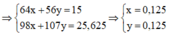
Bảo toàn electron => nNO2 = 2nCu + 3nFe + 6nS = 2,125mol
=> V = 47,6 lít

Đáp án B
Qui hỗn hợp X về dạng: Cu, Fe, S.
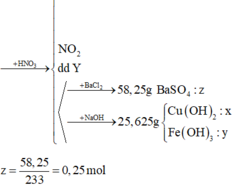
X + HNO3 dư → Muối (Fe3+, Cu2+, SO42-) + NO2
- Khi Y + BaCl2: Ba2+ + SO42- → BaSO4
=> nBaSO4 = 58,25: 233 = 0,25 mol = nS
- Khi Y + NaOH: Fe3+ → Fe(OH)3 ; Cu2+ → Cu(OH)2
nFe(OH)3 = nFe ; nCu(OH)2 = nCu
=> mtủa = 107nFe + 98nCu = 25,625g
Lại có: 56nFe + 64nCu = mX – mS = 23 – 0,25.32 = 15g
=> nFe = nCu = 0,125 mol
- Khi X + HNO3: Bảo toàn e: 3nFe + 2nCu + 6nS = nNO2
=> nNO2 = 3.0,125 + 2.0,125 + 6.0,25 = 2,125 mol
=> VNO2 = 2,125.22,4 = 47,6 lit



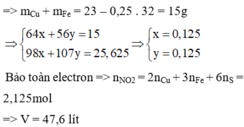
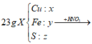

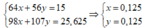

quy đổi hh thành fe,cu,s : 56x+64y+32z=6,48 (1)
Fe--->fe+3+3e
cu--->cu+2+2e
s--->s+4+4e
o2+4e---->2o2-
bte:3x+2y+0,28=0,45 (2)
giải 12--->x=0,03 ,y=0,04
phần :2 fe--->fe+3+3e
cu---->cu+2+2e
n+5+1e--->
s--->s+6
<=>0,03.3+0,04.2+0,07.6=nNO2====>v=13,216 l
ket tủa có :Fe(oH)3=nFe;cu(oh)2=nCu;BaSO4=nS--->m=23,44g