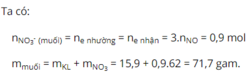Khi cho m (g) hỗn hợp gồm 3 kim loại Al, Mg, Cu tan vừa hết trong dd HNO3 loãng thu đc 3,36 lít khí NO (sp khử duy nhất, đktc) và dd X. Cô cạn cẩn thận dd X thu đc khối lượng muối khan là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Ta có nNO= 0,15 mol
QT nhận e:
NO3-+ 3e+ 4H+ → NO+ 2H2O
Ta có nNO3- trong muối= ne= 3.nNO= 3.0,15= 0,45 mol
→mmuối nitrat= mkim loại+ mNO3-trong muối= m+ 0,45.62= m+27,9 (gam)
Đáp án D

Coi B gồm : $Fe(x\ mol) ; O(y\ mol) \Rightarrow 56x + 16y = 8,32(1)$
$n_{NO} = \dfrac{2,688}{22,4} = 0,12(mol)$
Bảo toàn electron : $3n_{Fe} = 2n_O + 3n_{NO}$
$\Rightarrow 3x = 2y + 0,12.3(2)$
Từ (1)(2) suy ra x = 0,14 ; y = 0,03
$n_{Fe(NO_3)_3} = n_{Fe} = 0,14(mol)$
$\Rightarrow m = 0,14.242 = 33,88(gam)$

Đáp án A
Gọi x, y lần lượt là số mol Cu va Fe3O4 phản ứng
=>64x + 232y = 61,2 – 2,4 = 58,8 (1)
Sau phản ứng còn 2,4 gam kim loại đó là Cu, nên trong dung dịch có Cu2+, Fe2+
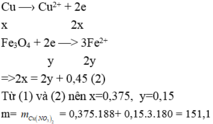

a) \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
0,1<----------------------------0,15
=> \(\%m_{Al}=\dfrac{0,1.27}{7,5}.100\%=36\%\)
\(\%m_{Cu}=100\%-36\%=64\%\)
b) \(n_{Cu}=\dfrac{7,5-0,1.27}{64}=0,075\left(mol\right)\)
PTHH: Cu + 2H2SO4 --> CuSO4 + SO2 + 2H2O
0,075------------------------>0,075
2Al + 6H2SO4 --> Al2(SO4)3 + 3SO2 + 6H2O
0,1----------------------------->0,15
=> VSO2 = (0,075 + 0,15).22,4 = 5,04 (l)

M trung bình hai khí = 37
Vì hai khí không mau và có một khí hóa nâu trong không khí nên hai khí này là NO và N2O
Đặt nNO =x, nN2O = y
Ta có hệ: x + y = 1,568/22,4 = 0,07
30x + 44y = 2,59
=> x = y = 0,035
Đặt nAl =a, nMg =b
Ta có hệ: 27a + 24b = 4,431
3a + 2b = 0,035.3 + 0,035.8
=> a=0,021, b = 0,161
a. % Al = 0,021.27/ 4,431.100% = 12,8%
% Mg = 100% -12,8% = 87,2%
b. nHNO3 = 4nNO + ***N2O = 0,49
=> CM = 0,49/ 0,2 = 2,45M
d. khối lượng muối = mAl(NO3)3 + mMg(NO3)2 = 28,301 gam
c. Để lượng kết tủa là nhỏ nhất thì nNaOH = 4nAl + 2nMg = 0,406 mol
mdd NaOH = 0,406.40/ 0,08 = 203 gam
V = 203/ 1,082 = 187,62 ml

\(n_{Zn}=a\left(mol\right),n_{Al}=b\left(mol\right)\)
\(n_{H_2}=\dfrac{8.96}{22.4}=0.4\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(2Al+6HCl\rightarrow2AlCl_3+H_2\)
\(n_{H_2}=a+1.5b=0.4\left(mol\right)\left(1\right)\)
\(m_{Muối}=m_{ZnCl_2}+m_{AlCl_3}=136a+133.5b=40.3\left(g\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.1,b=0.2\)
\(m_{hh}=0.1\cdot65+0.2\cdot27=11.9\left(g\right)\)
\(\%Zn=\dfrac{0.1\cdot65}{11.9}\cdot100\%=54.62\%\)
\(\%Al=100-54.62=45.38\%\)