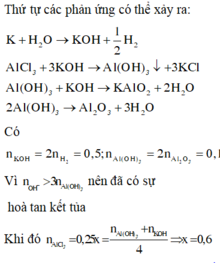cho 1 mẫu Na tác dụng hoàn toàn với 100ml dd AlCl3 thu được 5.6 lít (dktc) khí không màu và 1 kết tủa . lọc tách kết tủa rồi nung trong khong khí đến khối lượng không đổi thu được 5,1 game chất rắn , các phản ứng xảy ra hoàn toàn . tính nồng độ mol/l của dd ALCl3 ở dktc
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án : D
nAl2O3 = 0,05 mol => nAl(OH)3 = 0,1 mol
, nH2 = 0,25 mol
,nNa = nNaOH = 2nH2 = 0,5 mol
=> Kết tủa bị tan 1 phần => nAl(OH)3 = 4nAl3+ - nOH-
=> x = 1,5(M)

Đáp án B
Fe3++ 3OH- → Fe(OH)3
0,1 mol 0,1 mol
Al3++ 3OH- → Al(OH)3
Zn2++ 2OH- → Zn(OH)2
Do Al(OH)3 và Zn(OH)2 là hidroxit lưỡng tính nên bị tan trong NaOH dư
Kết tủa thu được có Fe(OH)3
2Fe(OH)3 → Fe2O3+ 3H2O
0,1 0,05 mol
mFe2O3 = 0,05.160 = 8 gam

Đáp án D
m gam K (x mol) + 0,25a mol AlCl3 → 0,25 mol H2↑ + ↓. Nung ↓ → 0,05 mol Al2O3
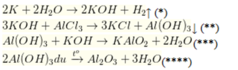
Theo (*) nH2 = 1/2x = 0,25 → nK = 0,5 mol.
Theo (**) nKOH = 3 × nAlCl3 = 3 × 0,25a = 0,75a mol;
nAl(OH)3 = 0,25a mol.
Theo (***) nAl(OH)3 dư = 0,05 × 2 = 0,1 mol
→ nAl(OH)3 phản ứng = 0,25a - 0,1
→ nKOH = 0,25a - 0,1
→ ∑nKOH = 0,75a + 0,25a - 0,1 = 0,5 → a = 0,6