một hỗn hợp khí A gồm 0,8 mol oxi, 0,2 mol cacbon oxit và 2 mol metan
a, cho biết khí A nặng hay nhẹ hơn không khí
b, tính phần trăm thể tích và phần trăm khối lượng mối khí trong A
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có:
Khối lượng của oxi trong A là : 0,8 . 16 = 12,8 (g)
Khối lượng của CO\(_2\)trong A là: 0,2 . 44 = 8,8 (g)
Khối lượng của CH\(_4\)trong A là : 2 . 16 = 32 (g)
=> Khối lượng của hỗn hợp A là : 12,8 + 8,8 + 32 = 53,6 (g)
% theo thể tích của O\(_2\) là: \(\frac{0,8.100\%}{0,2+0,8+2}=26,67\%\)
% theo thể tích của CO\(_2\)là: \(\frac{0,2.100\%}{0,8+0,2+2}=6,66\%\)
% theo thể tích của CH\(_4\)là: \(\frac{2.100\%}{0,8+0,2+2}=66,67\%\)

nCl2= 12,395 : 24,79 = 0,5 (mol)
nO2 = 37,185 : 24,79 = 1,5 (mol)
mO2 = 1,5 . 32 = 47=8 (G)
mCl2 = 0,5.71 = 35,5 (G)
%mO2 = \(\dfrac{8}{8+35,5}\) . 100% = 18,39%
%mCl2 = 100% - 18,39% = 81,61 %
Mhh = 32 + 71 = 103 (g/mol)
dMhh/29 = 103:29 = \(\dfrac{103}{29}\) = 3,55
=> hh nang hon KK 3,55 lan

Khối lượng của các khí:
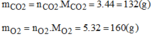
Thành phần phần trăm theo khối lượng:
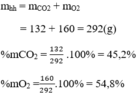
Thành phần phần trăm theo thể tích:
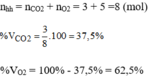

\(a.\)
\(n_{hh}=0.2+0.15+0.1=0.45\left(mol\right)\)
\(V_X=0.45\cdot22.4=10.08\left(l\right)\)
\(b.\)
\(m_X=0.2\cdot28+0.15\cdot71+0.1\cdot32=19.45\left(g\right)\)
\(c.\)
\(\overline{M}_X=\dfrac{19.45}{0.45}=43.22\left(g\text{/}mol\right)\)
\(d.\)
\(d_{X\text{/}kk}=\dfrac{43.22}{29}=1.4\)
Nặng hơn không khí 1.4 lần
câu này bạn áp dụng công thức tỉ khối hơi dA/kk = \(\frac{MA}{29}\) trong đó MA= ( 0,8*32 + 0,2*12 +2*16 )/(0,2 + 0,8 + 2) = 20
=> d = 20/29 => nhẹ hơn kk
còn câu b thì áp dụng công thức tính bình thường nhé , % V = % số mol ,
% m1chat= m1chat*100/mA