trong một bình kín chứa 500 mol hỗn hợp gồm N2 và H2 theo tỉ lệ số mol là 1:4. Với điều kiện thích hợp 2 khí trên phản ứng tạo thành 50 mol NH3. Tính hiệu suất phản ứng tạo thành NH3
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


1) N2 + 3H2 ------> 2NH3
x -------> 3x -----------> 2x
theo tỉ lệ đề bài chon n(N2) = 1 mol và n(H2) = 3 mol
gọi x là số mol N2 tham gia pứ
ta có pt đại số theo tỉ khối là:
M(A)/MB) = 0,6 <=> (m/4)/(1 - x + 3 - 3x + 2x) = 0,6 (m: khối lượng của hỗn hợp)
=> x = 0,8
H% = 0,8/1 *100 = 80%
2) ( Bạn đã cho thiếu đề rồi. Bây giờ tôi sẽ thêm vào 10 lit H2)
N2 + 3H2 ------> 2NH3

a) \(N_2+3H_2-^{t^o}\rightarrow2NH_3\)
3..........8
Lập tỉ lệ \(\dfrac{3}{1}>\dfrac{8}{3}\) => Tính theo số mol H2
\(n_{H_2\left(pứ\right)}=8.60\%=4,8\left(mol\right)\)
=> \(n_{NH_3}=\dfrac{4,8.2}{3}=3,2\left(mol\right)\)
=> \(V_{NH_3}=3,2.22,4=71,68\left(l\right)\)
b) Hỗn hợp A gồm N2 dư, H2 dư, NH3
\(n_{N_2\left(dư\right)}=3-\dfrac{4,8}{3}=1,4\left(mol\right)\)
\(n_{H_2\left(dư\right)}=8-4,8=3,2\left(mol\right)\)
\(M_A=\dfrac{3,2.2+1,4.28+3,2.17}{3,2+1,4+3,2}=12,82\)
=>dA/H2 \(=\dfrac{12,82}{2}=6,41\)

Đáp án D
Dễ thấy hiệu suất tính theo N2.
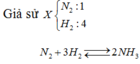
Bd: 1 4
Pu: 0,4→1,2→0,8
Sau: 0,6 2,8 0,8
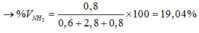

Đáp án D
Dễ thấy hiệu suất tính theo N2
Giả sử X N 2 : 1 H 2 : 4
![]()

\(N_2+3H_2\rightarrow2NH_3\)
So sánh:
\(\dfrac{n_{N_2}}{1}=2>\dfrac{n_{H_2}}{3}=1,333\)
-> Tính theo H2
\(n_{H_2}pư=75\%.4=3\left(mol\right)\)
\(\rightarrow n_{NH_3}=2\left(mol\right)\)
\(\rightarrow V_{NH_3}=2.22,4=44,8\left(l\right)\)
b. \(N_2+3H_2\rightarrow2NH_3\)
Bđ : 2 ..... 4 ..........
Pứ : a ....... 3a ........ 2a
Sau: (2-a) : (4-3a) : 2a
2-a+4-3a+2a = 4,5
=> a = 0,75 (mol)
%nH2 bị oxh = \(\dfrac{3.0,75}{4}.100\%=56,25\%\)

Đáp án C.
N2+ 3H2 ⇌ 2NH3
Vì  nên hiệu suất tính theo H2
nên hiệu suất tính theo H2
N2+ 3H2 ⇌ 2NH3
Ban đầu 0,5 0,5 mol
Phản ứng x/3 x 2x/3 mol
Sau pứ 0,2 mol
Ở trạng thái cân bằng có 0,2 mol NH3 tạo thành nên 2x/3= 0,2
→x=0,3


Chọn C
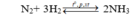
Giả sử phản ứng xảy ra với H = 100% → N 2 hết →Hiệu suất tính theo N 2 .
Đặt số mol N 2 ban đầu là x mol, n N 2 ban đầu = 4x mol;
Do hiệu suất phản ứng là 25% nên n N 2 pứ = 25%.x = 0,25x mol
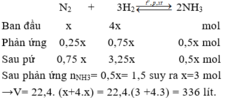


ban đầu nN2+ nH2=500 và nN2/nH2=1/4
=>nN2=100 mol và nH2=400 mol
N2 + 3H2 ---> 2NH3
ban đầu 100 400 0
phản ứng x 3x 2x
sau phản ứng (100-x ) ( 400-3x) 2x
lại có 50=2x=> x=25 => H%=( 25/100). 100%=25%.
Cảm ơn nhé