Hòa tan hoàn toàn 2g hỗn hợp hai kim loại đều hóa trị II và có số mol bằng nhau vào các ống nghiệm chứa dung dịch H2SO4,thu được 1,12 lít khí H2 ở đktc.Hỏi các kim loại trên là các kim loại nào trong số các kim loại sau đây: Mg , Ca , Ba , Zn , Fe , Cu, Ni ,Sn






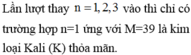
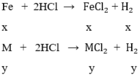
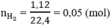
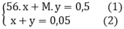
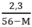
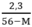 > 0 → 56 – M > 0 ⇒ M < 56
> 0 → 56 – M > 0 ⇒ M < 56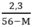 < 0,05 → 2,3 < 0,05(56 – M) → M < 10
< 0,05 → 2,3 < 0,05(56 – M) → M < 10


Gọi 2 kim loại cần tìm là: A và B
PTHH: A + H2SO4 → ASO4 + H2
B + H2SO4 → BSO4 + H2
(Gọi a là số mol của cả 2 kim loại A , B vì 2 kim loại có số mol bằng nhau.)
Tổng số mol của hiđrô là: 1,12 : 22,4 = 0,05(mol)
=> Số mol hiđrô ở pt (1) = số mol hiđrô ở pt (2) = 0,05 / 2 = 0,025 (mol)
=> Số mol của A = Số mol của B = 0,025
=> 0,25 ( MA + MB ) = 2(gam)
=> MA + MB = 80
Mà trong các kim loại nói trên chỉ có 2 kim loại là Mg và Fe thoả mãn điều kiện (vì 56 + 24 = 80)
=> 2 kim lại đó là Mg vad Fe