Hòa tan 3,6 gam sắt (2) oxit vào dung dịch clohidric dư.Tìm khối lượng muối clorua thu được.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) Fe + 2HCl --> FeCl2 + H2
b) \(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
_____0,1--------------->0,1---->0,1
=> mFeCl2 = 0,1.127 = 12,7(g)
c) VH2 = 0,1.22,4 = 2,24(l)
\(n_{Fe}=\dfrac{5,6}{56}=0,1(mol)\\ a,Fe+2HCl\to FeCl_2+H_2\\ \Rightarrow n_{FeCl_2}=n_{H_2}=0,1(mol)\\ a,m_{FeCl_2}=0,1.127=12,7(g)\\ b,V_{H_2}=0,1.22,4=2,24(l)\)

Đáp án C
Ta có:
![]()
ne nhường = 2.nZn = 0,4 mol > ne nhận = 10.nN2 = 0,2 mol → phản ứng tạo thành NH4NO3.
![]()
(vì khi tạo thành NH4NO3: N + 8e → N)
Khối lượng muối trong dung dịch X là = 180.0,2 + 80.0,025 = 39,80 gam
Lưu ý: Đề bài không nói thu được khí X duy nhất nên có thể có muối NH4NO3 tạo thành.

Đáp án C
Ta có:
![]()
ne nhường = 2.nZn = 0,4 mol > ne nhận = 10.nN2 =0,2 mol → phản ứng tạo thành NH4NO3.
![]()
(vì khi tạo thành NH4NO3: N + 8e → N)
Khối lượng muối trong dung dịch X là = 180.0,2 + 80.0,025 = 39,80 gam

a/
\(Fe_2O_3\left(x\right)+6HCl\left(6x\right)\rightarrow2FeCl_3\left(2x\right)+3H_2O\)
\(CuO\left(y\right)+2HCl\left(2y\right)\rightarrow CuCl_2\left(y\right)+H_2O\)
Gọi số mol của Fe2O3 và CuO lần lược là: x, y
Ta có: \(\left\{\begin{matrix}160x+80y=64\\162,5.2x+135y=124,5\end{matrix}\right.\)
\(\left\{\begin{matrix}x=0,3\\y=0,2\end{matrix}\right.\)
\(\%Fe_2O_3=\frac{160.0,3}{64}=75\%\)
\(\Rightarrow\%CuO=100\%-75\%=25\%\)
b/ \(n_{HCl}=6.0,3+2.0,2=2,2\)
\(m_{HCl}=2,2.36,5=80,3\)
\(m_{ddHCl}=\frac{80,3}{0,2}=401,5\)
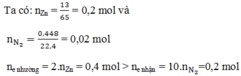
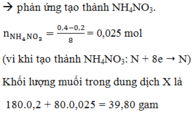

nFeO=\(\frac{3,6}{56+16}=0.05\)mol
PTHH
: FeO+ 2HCl--> FeCl2+H2O
0,05--------------> 0,05
khói lượng muối clorua:
= 0,05.( 56+35.5.2)=6,35 g