Dẫn khí CO2 điều chế được bằng cách cho 10 gam CaCO3 tác dụng với dung dịch HCl dư đi vào dung dịch có chứa 8 gam NaOH. Khối lượng muối natri điều chế được (cho Ca = 40, C=12, O =16)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


nNaOH= 1,5mol
=> Tỉ lệ nNaOH/nCO2 = 1,5 => Ra hai muối: NaHCO3 và Na2CO3
Bạn có thể gọi số mol hai muối, lập hệ rồi giải ra như bình thường nhưng nhận xét thấy tỉ lệ là 1,5( là TB cộng) => số mol hai muối bằng nhau và = 1/2 nCO2 = 0,5 mol
=> m muối =95g

Tính khối lượng muối
Khối lượng NaOH có trong dung dịch :
m NaOH = 40x50/100 = 20(gam) ứng với số mol là
m NaOH = 20/40 = 0,5 mol
Số mol NaOH lớn gấp hớn 2 lần số mol CO 2 , vậy muối thu được sẽ là Na 2 CO 3
CO 2 + 2NaOH → Na 2 CO 3 + H 2 O
Theo phương trình hoá học, ta có :
n Na 2 CO 3 = n CO 2 = 0,1 mol
Khối lượng muối cacbonat thu được : m Na 2 CO 3 = 106 x 0,1 = 10,6g

CaCO3 + 2HCl -> CaCl2 + CO2 + H2O (1)
NaOH + CO2 -> NaHCO3 (2)
2NaOH + CO2 -> Na2CO3 + H2O (3)
nCaCO3=0,1(mol)
Từ 1:
nCO2=nCaCO3=0,1(mol)
Nếu tỉ lệ \(\dfrac{n_{NaOH}}{n_{CO2}}=1\) thì xảy ra PT 2
TỪ 2:
nNaHCO3=nCO2=0,1(mol)
mNaHCO3=0,1.84=8,4(g)
Nếu tỉ lệ \(\dfrac{n_{NaOH}}{n_{CO2}}=2\) thì xảy ra PT 3
Từ 3:
nNa2CO3=nCO2=0,1(mol)
mNa2CO3=106.0,1=10,6(g)
Vậy 8,4\(\le\)mmuối tạo thành\(\le\)10,6
nCaCO3=10/100=0,1(mol)
pt: CaCO3+2HCl--->CaCl2+CO2+H2O
0,1______________________0,1(mol)
CO2+2NaOH--->Na2CO3+H2O
0,1______________0,1
mNa2CO3=0,1.106=10,6(g)

a) CaCO3+2HCl=>CaCl2+H2O+CO2
n CaCO3=10/100 = 0,1 mol
theo phương trình : n CO2 = n CaCO3 = 0,1 mol
=> V CO2 = 0,1*22,4 = 2,24 lít
b) CO2+2NaOH => Na2CO3+H2O
có thể xảy ra phản ứng :
Na2CO3+CO2+H2O=>2NaHCO3
m NaOH = 25*0,4 = 10 gam
=> n NaOH = 10/40 = 0,25 mol
mà nếu theo phương trình đầu tiên của câu b:
n CO2 = 1/2 n NaOH = 1/2*0,25 = 0,125 mol
mà thực tế n CO2 có 0,1 mol
=> n CO2 hết, n NaOH dư
=> chỉ tạo ra 1 muối là Na2CO3
n Na2CO3 = n CO2 = 0,1 mol
=> m Na2CO3 = 0,1*106=10,6 gam

a+b) PTHH: \(CaCO_3+2HCl\rightarrow CaCl_2+H_2O+CO_2\uparrow\)
Ta có: \(n_{CaCO_3}=\dfrac{10}{100}=0,1\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{HCl}=0,2\left(mol\right)\\n_{CO_2}=0,1\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{HCl}=0,2\cdot36,5=7,3\left(g\right)\\V_{CO_2}=0,1\cdot22,4=2,24\left(l\right)\end{matrix}\right.\)
c) Ta có: \(\left\{{}\begin{matrix}n_{CO_2}=0,1\left(mol\right)\\n_{NaOH}=\dfrac{50\cdot40\%}{40}=0,5\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\) Tạo muối trung hòa, bazơ dư, tính theo CO2
Bảo toàn Cacbon: \(n_{Na_2CO_3}=n_{CO_2}=0,1\left(mol\right)\) \(\Rightarrow m_{Na_2CO_3}=0,1\cdot106=10,6\left(g\right)\)

PTHH
CaCO3 + 2HCl--> CaCl2 + CO2 + H2O
\(\frac{10}{100}\) 0.1 mol
CO2 + 2NaOH--> Na2CO3 + H2O
0.1 0.1 mol
=> m muối = 0.1 * 106 =10.6 g

CaCO3 + 2HCl → CaCl2 + H2O + CO2
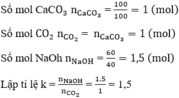
K = 1,5 → phản ứng tạo hai muối NaHCO3 và Na2CO3
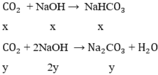
Gọi x, y lần lượt là số mol NaHCO3 và Na2CO3
Theo bài ra ta có hệ
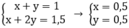
Khối lượng NaHCO3 m = 84.0,5 = 42 (g)
Khối lượng Na2CO3 m = 106.0,5 = 53 (g)
Tổng khối lượng muối thu được sau phản ứng là: 42 + 53 = 95 (g)
Thành phần % theo khối lượng các chất
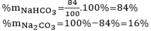
C