Cho m gam 1 ancol no đơn chức X qua bình đựng CuO (dư) đun nóng. Sau khi phản ứng hoàn toàn, khối lượng của chất rắn trong bình giảm 0,32 gam. Hỗn hợp hơi thu được có tỉ khối đối với hidro là 15,5. Giá trị của m là? Mong các anh chị giải nhanh dùm em với
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
Hướng dẫn
Phương trình phản ứng:

Khối lượng chất rắn giảm = mO phản ứng
=> nO = nCuO = 0,32 : 16 = 0,02 mol
Do phản ứng xảy ra hoàn toàn nên ancol hết, sản phẩm chỉ có andehit và hơi nước.
Ta có:
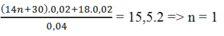
=> m = 0,02.46 = 0,92 gam.

Đáp án D
Hỗn hợp hơi gồm CnH2nO và H2O
=> nCnH2nO = nH2O= nO = 0,02
=>M = (18n+16 + 18)/2 = 15,5.2 => n = 2
=>X là C2H5OH (0,02 mol)
=> mX = 0,92

Đáp án D
Hỗn hợp hơi gồm CnH2nO và H2O
=> nCnH2nO = nH2O= nO = 0,02
=>M = (18n+16 + 18)/2 = 15,5.2
=> n = 2
=>X là C2H5OH (0,02 mol)
=> mX = 0,92

Đáp án A
RCH2OH + [O] => RCHO + H2O
n[O] = 0,32/16 = 0,02
BT kl ta có m = 0,04 * (15,5*2) – 0,32 = 0,92(g)

Đáp án D
Hỗn hợp hơi gồm CnH2nO và H2O
=> nCnH2nO = nH2O = nO = 0,02
=>M = (18n+16 + 18)/2 = 15,5.2 => n = 2
=>X là C2H5OH (0,02 mol)
=> mX = 0,92

Đáp án A
Hướng dẫn:
Đặt công thức phân tử của ancol no, đơn chức X là : CnH2n + 2O
Phương trình phản ứng :
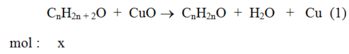
Khối lượng chất rắn giảm = mCuO – mCu = 80x – 64x = 0,32 Þ x = 0,02
(Áp dụng sơ đồ đường chéo):
Hỗn hợp hơi gồm CnH2nO và H2O có khối lượng mol trung bình là : 15,5.2 = 31 gam/mol.
Áp dụng sơ đồ đường chéo ta có :
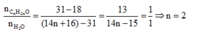
Vậy khối lượng của X là:
m = (14n + 18).0,02 = (14.2 + 18).0,02 = 0,92 gam.
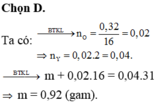
m giảm chính là kl oxi
=>nO=n(andehit)=nH2O=0,02 mol
=>n(sản phẩm )=0,04 mol =>msau=0,04.2.15,5=1,24 gam
=> m t=ms-mgiảm=1,24-0,32=0,92 gam
khối lượng rắn giàm là khối lượng của oxi tham gia p/ư oxi hóa ancol
n O = 0,32: 16 = 0,02 .
Giả sử ancol bậc 1 để viết p/ư minh họa
R-CH2OH + CuO ---> RCHO + H2O + Cu
R-CH2OH + O ---> RCHO + H2O
0.02 0,02 0,02 0,02
M hh hơi = 15,5.2 = 31 ; n hh hơi = 0,04 => m hh hơi = 0,04. 31 = 1,24 gam.
Bảo toàn khối lượng để tính m ancol = m hh hơi - m O
m = 1,24 - 0,32 = 0,92 gam