X là đồng đẳng của axetilen. Khi cho m gam X vào dd 500ml AgN03 1M(trong NH3) thì thu được 40,25 g kết tủa và nồng độ AgN03 giảm đi một nửa. Tìm CTPT, viết CTCT của X. Gọi tên thường và tên thay thế
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án C
Pt pư:
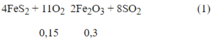
Ta có: nBaC03 = 0,15 mol
nKOH = 0,1 mol ⇒ nBa2+ = 0,15 mol ; nOH- = 0,4 mol
Khi cho SO2 vào dung dịch Y thu được 21,7 (g) BaSO3. Cho Y tác dụng với dung dịch NaOH thấy xuất hiện thêm kết tủa, chứng tỏ trong dung dịch Y có ion HSO3-.
Vì: Ba2+ + HSO3- + OH- " BaSO3 + H2O
Ta có: nBaC03 = 0,1 mol
Ptpứ:
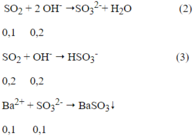
Ta có: nOH- = 0,4 - 0,2 = 0,2 mol
Theo ptpư (2), (3) ta có: n SO2= 0,1 + 0,2 = 0,3 mol
Theo ptpư (1) ta có: n FeS2 = ½ n SO2= 0,15 mol ⇒ m FeS2 = 120.0,15 = 18(g)

Đáp án A
Số mol Fe = 0,02 mol; số mol Cu = 0,03 mol; số mol H+ = 0,4 mol;
số mol NO3- = 0,08 mol
Các phản ứng xảy ra:
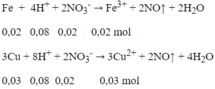
Sau 2 phản ứng trên, trong dung dịch X có 0,02 mol Fe3+; 0,03 mol Cu2+ và 0,24 mol H+ dư, ngoài ra còn có ion NO3- và SO42-. Tuy nhiên chỉ có 3 loai ion đầu là phản ứng với OH-.
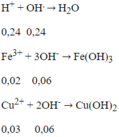
Tổng số mol OH- = 0,24 + 0,06 + 0,06 = 0,36 mol
→ V = 360ml

Đáp án C
Ta có: n C 6 H 12 O 6 = 1 2 . n Ag = 1 2 . 2 , 16 108 = 0 , 01 mol
→ CM(glucozơ) = n C 6 H 12 O 6 V C 6 H 12 O 6 = 0 , 01 50 . 10 - 3 = 0 , 2 M

Đáp án B
Zn có tính khử mạnh hơn Fe, Zn sẽ phản ứng với dung dịch CuSO4 trước.
Theo đề: hỗn hợp rắn Z phản ứng với dung dịch H2SO4 loãng thu được 1 muối duy nhất → trong hỗn hợp rắn Z có Cu và Fe dư. Vậy mFe dư = 0,28 (g) và mCu = 2,84 - 0,28 = 2,56 (g)
Ta có: khối lượng hỗn hợp X phản ứng với Cu2+ = 2,7 - 0,28 = 2,42 (g)
Gọi nZn = x mol; nFe pư = y mol
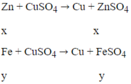
Ta có hệ:
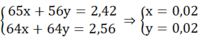
mFe ban đầu = 0,02.56 + 0,28 = 1,4 (g)
![]()
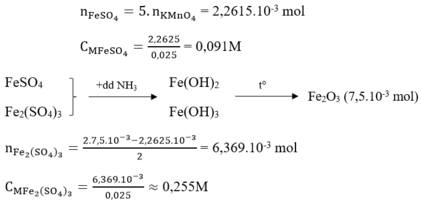
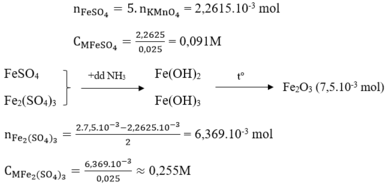
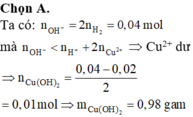
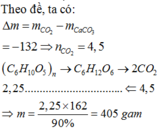
X là ankin có công thức: CnH2n-2.
2X + Ag2O (sinh ra từ hh AgNO3/NH3) ---> 2R-CAg (kết tủa) + H2O
Nồng độ giảm đi một nửa tức là AgNO3 đã phản ứng 0,5/2 = 0,25 mol.
Suy ra: n(kết tủa) = 0,25 mol. Hay R-CAg = 40,25/0,25 = 161. Vậy: R = 161 - 12 - 108 = 41 (C3H5).
Như vậy ankin cần tìm là C4H6. Có CTCT là: CH3 - CH2 - C\(\equiv\)CH (but-1-in).