đốt hoàn toàn 14,5 gam Ankan A được 22,5 gam H2O .tìm ctpt và Vkk đã đốt
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) \(n_{CO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Bảo toàn C: nC = 0,4 (mol)
=> \(n_H=\dfrac{5,8-0,4.12}{1}=1\left(mol\right)\)
Xét nC : nH = 0,4 : 1 = 2 : 5
=> CTPT: (C2H5)x
Mà CTPT của X có dạng CnH2n+2
=> x = 2
=> CTPT: C4H10
b)
PTHH: 2C4H10 + 13O2 --to--> 8CO2 + 10H2O
0,65<-------0,4------->0,5
=> \(m_{H_2O}=0,5.18=9\left(g\right)\)
c) \(V_{O_2}=0,65.22,4=14,56\left(l\right)\)

Đáp án C
Đốt cháy Y cũng là đốt cháy X.
X + O2 → 0,06 mol CO2 + 0,08 mol H2O.
• nXn = H2O - nCO2 = 0,08 - 0,06 = 0,02 mol.
X có số nguyên tử C = 0,06 : 0,02 = 3; số nguyên tử H = 0,08 x 2 : 0,02 = 8 → X là C3H8.
→ hhY gồm C3H8 dư; CH4 và C2H6; mX = 0,02 x 44 = 0,88 gam.
Theo BTKL: mY = mX = 0,88 gam → nY = 0,88 : 27,5 = 0,032 mol
→ nankan phản ứng = 0,032 - 0,02 = 0,012 mol
⇒ H = 0 , 012 0 , 02 = 60 %


Đặt công thức tổng quát của hiđrocacbon là C x H y .
Ta có:
x : y = n C : n H = m C O 2 44 : m H 2 O 9 = 1,76 44 : 0,9 9 = 0,04 : 0,1 = 2 : 5
Vậy công thức đơn giản nhất của A là C 2 H 5 n
Mà D A = 2 , 59 g / l ⇒ M A = 2 , 59 . 22 , 4 = 58 g
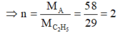
Vậy CTPT của A là C 4 H 10 .
⇒ Chọn D.

Chọn đáp án B
Đốt cháy anken luôn thu được nCO2 = nH2O
Đốt cháy ankan luôn thu được nCO2 < nH2O
=> Sự chênh lệch số mol CO2 và H2O chính là số mol của ankan.
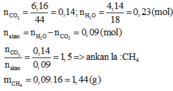

a) MX = 146g/mol
VCO2 : VH2O = 6 : 5
=> nC : nH = 3 : 5
=> CTĐGN: (C3H5Oa)n
→ (41 + 16a).n = 146 → (a; n) = (4; 2) → X: C6H10O4
b) C6H10O4 + 6,5O2 → 6CO2 + 5H2O
0,05 0,325
=> p = 7,3g
c)
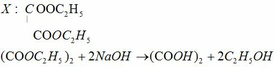
nH2O = \(\dfrac{1}{2}\)nH = 1,25 (mol) \(\rightarrow\) nH = 2,5 (mol)
mC = 14,5 - 2,5 = 12 (g) \(\rightarrow\) nC = 1 (mol)
\(\dfrac{n_C}{n_H}\) = \(\dfrac{1}{2,5}\)= \(\dfrac{2}{5}\) \(\rightarrow\) C4H10