Ête là gì ? Cho biết nhiệt độ nóng chảy, nhiệt độ sôi của ête ? Vẽ đồ thị ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


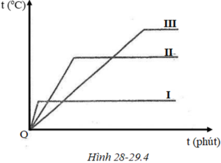
I: Ete II: rượu III: nước
Căn cứ đường biểu diễn đã cho đoạn nằm ngang ứng với chất lỏng sôi. Vì thế nhiệt độ sôi của nước là 100°C cao nhất nên phải là đường III, nhiệt độ sôi của ê-te là 35 ° C nên phải là đường I. Vì nhiệt độ sôi của rượu là 80°C nên phải là đường II.

I: Ete
II: rượu
III: nước
Căn cứ đường biểu diễn đã cho đoạn nằm ngang ứng với chất lỏng sôi. Vì thế nhiệt độ sôi của nước là 100oC cao nhất nên phải là đường III, nhiệt độ sôi của ê-te là 35oC nên phải là đường I. Vì nhiệt độ sôi của rượu là 80oC nên phải là đường II.

Đáp án: A
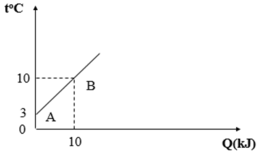
- Đoạn AB trên đồ thị nước tăng nhiệt độ từ 3 0 C lên 10 0 C . Trong giai đoạn này nhiệt lượng mà nước nhận vào là 10kJ. Như vậy để tăng thêm 1 0 C thì nhiệt lượng nước nhận vào là:
10 : 7 = 1,43 (kJ)
- Nhiệt lượng cần cung cấp để đun sôi nước (từ 3 0 C ) là:
1,43.(100-3) = 139(kJ)

Lời giải:
Độ chênh lệch giữa nhiệt độ sôi và nhiệt độ nóng chảy của thủy ngân là:
$357-(-39)=357+39=396$ (độ C)

Do đường kính của hai ống mao dẫn khác nhau nên khi nhúng vào chất lỏng, cột chất lỏng dâng lên trong hai ống sẽ khác nhau. Hiệu số độ cao của các cột chất lỏng đó còn phụ thuộc vào bản chất của chất lỏng đó.
Đối với ête, hiệu số đó bằng:
![]()
Đối với dầu hỏa, hiệu số đó bằng:
![]()
Từ (1) và (2) :
![]()

Lực Van der Waals là một loại tương tác giữa các phần tử có tiếp xúc với nhau, được đặt tên của nhà vật lý người Hà Lan Johannes Diderik van der Waals, mô tả một loại tương tác phụ thuộc vào khoảng cách giữa các phần tử, công bố đầu tiên vào năm 1873. Các phần tử tham gia vào lực này thường là phân tử.
Thực chất, lực Van der Waals là lực tĩnh điện, thường xuất hiện giữa các phân tử chất khí, khí hóa lỏng hoặc hóa rắn, và trong hầu hết các chất lỏng và chất rắn hữu cơ.
- Tương tác van der Waals làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của các chất. Khi khối lượng phân tử tăng, kích thước phân tử tăng thì tương tác van der Waals tăng.
-Tương tác van der Waals làm tăng nhiệt độ sôi và nhiệt độ nóng chảy. ⟹ Khí hiếm có nhiệt độ nóng chảy thấp nhất là He và cao nhất là Xe.

Đáp án D
X tan ít ở nhiệt độ thường nhưng tan vô hạn ở nhiệt độ 80oC → Phenol
Y có nhiệt độ nóng chảy rất cao → Y là amino axit
(Z có nhiệt độ nóng chảy < 0oC → không thể là amino axit)

Đáp án D
X tan ít ở nhiệt độ thường nhưng tan vô hạn ở nhiệt độ 80oC → Phenol
Y có nhiệt độ nóng chảy rất cao → Y là amino axit
(Z có nhiệt độ nóng chảy < 0oC → không thể là amino axit)