Cho 17,2 gam hỗn hợp gồm K và K2O tác dụng với nước dư. Sau phản ứng thu được 2, 24 lít khí (đktc). Viết các PTHH xảy ra và gọi tên sản phẩm Tính khối lượng K; K2O có trong hỗn hợp ban đầu. (K = 39; O = 16; H = 1)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a, \(Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\)
\(BaO+H_2O\rightarrow Ba\left(OH\right)_2\)
Ba(OH)2: bari hydroxit
H2: hydro
b, Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Theo PT: \(n_{Ba}=n_{H_2}=0,2\left(mol\right)\Rightarrow m_{Ba}=0,2.137=27,4\left(g\right)\)
\(\Rightarrow m_{BaO}=42,7-27,4=15,3\left(g\right)\)

\(n_{H_2}=\dfrac{2,479}{24,79}=0,1\left(mol\right)\)
PTHH:
2K + 2H2O ---> 2KOH + H2
0,2<---------------0,2<----0,1
=> \(\left\{{}\begin{matrix}m_K=0,2.39=7,8\left(g\right)\\m_{K_2O}=12,5-7,8=4,7\left(g\right)\end{matrix}\right.\)
\(n_{K_2O}=\dfrac{4,7}{94}=0,05\left(mol\right)\)
PTHH: K2O + H2O ---> 2KOH
0,05-------------->0,1
=> mKOH = (0,2 + 0,1).56 = 16,8 (g)

\(n_{H2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
a) Pt : \(2Na+2H_2O\rightarrow2NaOH+H_2|\)
2 2 2 1
a 0,5a
\(2K+2H_2O\rightarrow2KOH+H_2|\)
2 2 2 1
b 0,5b
b) Gọi a là số mol của Na
b là số mol của K
\(m_{Na}+m_K=10,1\left(g\right)\)
⇒ \(n_{Na}.M_{Na}+n_K.M_K=10,1g\)
⇒ 23a + 39b = 10,1g (1)
Theo phương trình : 0,5a + 0,5b = 0,15(2)
Từ(1),(2), ta có hệ phương trình :
23a + 39b = 10,1g
0,5a + 0,5b = 0,15
⇒ \(\left\{{}\begin{matrix}a=0,1\\b=0,2\end{matrix}\right.\)
\(m_{Na}=0,1.23=2,3\left(g\right)\)
\(m_K=0,2.39=7,8\left(g\right)\)
0/0Na = \(\dfrac{2,3.100}{10,1}=22,77\)0/0
0/0K = \(\dfrac{7,8.100}{10,1}=77,23\)0/0

\(a,n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ PTHH:2K+2H_2O\rightarrow2KOH+H_2\uparrow\\ Theo.pt:n_K=2n_{H_2}=2.0,1=0,2\left(mol\right)\\ m_K=0,2.39=7,8\left(g\right)\\ m_{K_2O}=17,2-7,8=9,4\left(g\right)\\ b,n_{CuO\left(bđ\right)}=\dfrac{12}{80}=0,15\left(mol\right)\\ PTHH:CuO+H_2\underrightarrow{t^o}Cu+H_2O\\ LTL:0,15>0,1\Rightarrow Cu.dư\)
Gọi nCuO (pư) = a (mol)
=> nCu = a (mol)
mchất rắn sau pư = 80(0,15 - a) + 64a = 10,8
=> a = 0,075 (mol)
=> nH2 (pư) = 0,075 (mol)
\(H=\dfrac{0,075}{0,1}=75\%\)

`2Fe + 6H_2 SO_[4(đ,n)] -> Fe_2(SO_4)_3 + 3SO_2 \uparrow + 6H_2 O`
`0,05` `0,15` `0,025` `(mol)`
`Cu + 2H_2 SO_[4(đ,n)] -> CuSO_4 + SO_2 \uparrow + 2H_2 O`
`0,225` `0,45` `0,225` `(mol)`
`n_[SO_2]=[6,72]/[22,4]=0,3(mol)`
Gọi `n_[Fe]=x` ; `n_[Cu]=y`
`=>` $\begin{cases} \dfrac{3}{2}x+y=0,3\\56x+64y=17,2 \end{cases}$
`<=>` $\begin{cases}x=0,05\\y=0,225 \end{cases}$
`@m_[Fe_2(SO_4)_3]=0,025.400=10(g)`
`@m_[CuSO_4]=0,225.160=36(g)`
`@m_[dd H_2 SO_4]=[(0,15+0,45).98]/80 .100=73,5(g)`
Sửa đề: 80% ---> 98% (80% chưa đặc nên không giải phóng SO2 được)
Gọi \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{Cu}=b\left(mol\right)\end{matrix}\right.\)
\(\rightarrow56a+64b=17,2\left(1\right)\)
PTHH:
\(2Fe+6H_2SO_{4\left(đặc,nóng\right)}\rightarrow Fe_2\left(SO_4\right)_3+3SO_2\uparrow+6H_2O\)
a------>3a------------------->0,5a--------------->1,5a
\(Cu+2H_2SO_{4\left(đặc,nóng\right)}\rightarrow CuSO_4+SO_2\uparrow+2H_2O\)
b----->2b------------------->b------------->b
\(\rightarrow1,5a+b=\dfrac{6,72}{22,4}=0,3\left(2\right)\)
Từ \(\left(1\right)\left(2\right)\rightarrow\left\{{}\begin{matrix}a=0,05\left(mol\right)\\b=0,225\left(mol\right)\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}m_{Fe_2\left(SO_4\right)_3}=0,5.0,05.400=10\left(g\right)\\m_{CuSO_4}=0,225.160=36\left(g\right)\\m_{ddH_2SO_4}=\dfrac{\left(0,05.3+0,225.2\right).98}{98\%}=60\left(g\right)\end{matrix}\right.\)

a) Các phương trình phản ứng:
C2H4 + Br2 → C2H4Br2
C2H2 + 2Br2 → C2H2Br4
C2H2 + Ag2O → C2Ag2 + H2O
Hay
C2H2 + 2AgNO3 + 2NH3 → C2Ag2 + 2NH4NO3
b) Gọi a, b, c lần lượt là số mol của CH4, C2H4, C2H2 trong 4,3gam hỗn hợp T.
– Số mol Br2 = 0,15 (mol); số mol kết tủa = số mol C2H2 = 0,075 (mol); số mol T = 0,3 (mol). Do đó nT = 4nC2H2
– Ta có hệ phương trình:
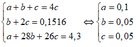
– Suy ra % thể tích mỗi khí trong T:
%VCH4 = 50%; %VC2H2 = %VC2H4 = 25%

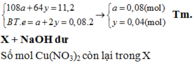

`2K+2H_2O->2KOH+H_2` (sp: Kali hidroxit, Hidro)
0,2---------------------------0,1 mol
`K_2O+H_2O->2KOH`
`n_(H_2)=((2,24)/(22,4))=0,1 mol`
`->m_(K)=0,2.39=7,8g`
`->m_(K_2O)=17,2-7,8=9,4g`