Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) n glucozo = 54/180 = 0,3(mol)
n glucozo pư = 0,3.80% = 0,24(mol)
$C_6H_{12}O_6 \xrightarrow{t^o} 2CO_2 +2 C_2H_5OH$
n C2H5OH = 2n glucozo = 0,48(mol)
m C2H5OH = 0,48.46 = 22,08(gam)
b)
$C_2H_5OH + O_2 \xrightarrow{men\ giấm} CH_3COOH + H_2O$
n CH3COOH = n C2H5OH = 0,48(mol)
C% CH3COOH = 0,48.60/500 .100% = 5,76%

V C 2 H 5 OH = 50.4/100 = 2l
→ m C 2 H 5 OH = 2.1000.0,8 = 1600g
Phương trình hóa học :
C 2 H 5 OH + O 2 → CH 3 COOH + H 2 O
46 gam 60 gam
1600 gam x
x = 1600x60/46
Vì hiệu suất đạt 80% → m CH 3 COOH = 1600.60.80/(46.100) = 1669,6g
→ m giấm = 1669,6/5 x 100 = 33392 (gam) = 33,392 kg

\(a,C_2H_5OH+O_2\left(men.giấm\right)\rightarrow CH_3COOH+H_2O\\ V_{C_2H_5OH\left(ng.chất\right)}=\dfrac{2,875}{10}=0,2875\left(l\right)=287,5\left(ml\right)\\ m_{C_2H_5OH}=287,5.0,8=230\left(g\right)\\ n_{C_2H_5OH}=\dfrac{230}{46}=5\left(mol\right)\\ n_{CH_3COOH\left(LT\right)}=n_{C_2H_5OH}=5\left(mol\right)\\ n_{CH_3COOH\left(TT\right)}=5.80\%=4\left(mol\right)\\ m_{CH_3COOH\left(TT\right)}=4.60=240\left(g\right)\\ b,m_{dd.giấm}=\dfrac{240.100}{5}=4800\left(gam\right)\)

Đáp án: B
Ta có: trong 5 lít rượu 40 o có 2 lít rượu nguyên chất. Vậy khối lượng rượu etylic có trong 5 lít rượu 40 o là:
m = D.V = 0,8.2.1000 = 1600 gam
Vì hiệu suất của phản ứng đạt 92% nên khối lượng của rượu etylic thực tế bị lên men là: 1600.0,92 = 1472 gam
Số mol rượu etylic thực tế bị lên men là: n = 1472 46 = 32 m o l
PTHH: C 2 H 5 O H + O 2 → m e n g i a m C H 3 C O O H + H 2 O
32 mol → 32 mol
=> khối lượng axit axetic thu được là: 32.60 = 1920 gam

$V_{C_2H_5OH\,nguyên\,chất}=\frac{5.40}{100}=2(l)=2000(ml)$
$\to m_{C_2H_5OH}=2000.0,8=1600(g)$
Vì $H=92\%$
$\to n_{C_2H_5OH(pứ)}=\frac{1600.92\%}{46}=32(mol)$
$C_2H_5OH+O_2\xrightarrow{\rm men\,giấm}CH_3COOH+H_2O$
Theo PT: $n_{CH_3COOH}=n_{C_2H_5OH}=32(mol)$
$\to m_{CH_3COOH}=32.60=1920(g)$

\(n_{C_6H_{12}O_6}=\dfrac{45}{180}=0,25mol\)
\(C_6H_{12}O_6\underrightarrow{lênmen}2C_2H_5OH+2CO_2\)
0,25 0,5 0,5
\(C_2H_5OH+O_2\underrightarrow{mengiấm}CH_3COOH+H_2O\)
0,5 0,5
\(C_{M_{CH_3COOH}}=\dfrac{0,5}{1}=0,5M\)
\(n_{C_6H_{12}O_6}=\dfrac{45}{180}=0,25\left(mol\right)\)
PTHH:
C6H12O6 --men rượu--> 2CO2 + 2C2H5OH
0,25-------------------------------------->0,5
C2H5OH + O2 --men giấm--> CH3COOH + H2O
0,5------------------------------------->0,5
\(\rightarrow C_{M\left(CH_3COOH\right)}=\dfrac{0,5}{1}=0,5M\)

Trong 50 lít rượu etylic 4 ° có 50/100 x 4 = 2(l) rượu nguyên chất
Vậy khối lượng rượu etylic có trong 50 lít rượu 4 ° là :
2 x 1000 x 0,8 = 1600 (gam)
Vì hiệu suất đạt 92% nên khối lượng rượu đã lên men là 1600x92/100 = 1472 (gam)
Số mol rươu đã lên men là 1472/46 = 32 (mol)
Phản ứng lên men :
C 2 H 5 OH + O 2 → CH 3 COOH + H 2 O
Vậy khối lượng của CH 3 COOH tạo ra là :
60 x 32 = 1920 (gam).
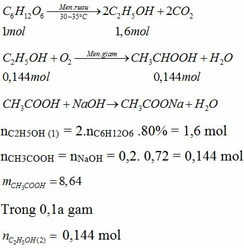

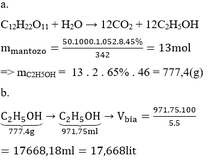
ĐỢI XÍUUUUUUUUUU ! Em hỏi mẹ em đã ( mẹ em GV dạy Hoá ó )
Bài toán:
Cho 90g glucose lên men rượu thu được 19,832 lít CO₂ ở điều kiện chuẩn và dung dịch X.
Câu hỏi:
Giải thích:
Phương trình hóa học của quá trình lên men rượu của glucose là:
�6�12�6→Enzyme2�2�5��+2��2C6H12O6Enzyme2C2H5OH+2CO2
Điều này có nghĩa là 1 phân tử glucose (C₆H₁₂O₆) tạo ra 2 phân tử ethanol (C₂H₅OH) và 2 phân tử CO₂.
Tuy nhiên, thực tế thu được 19.832 lít CO₂. Vì vậy, hiệu suất của quá trình lên men là:
Hiệu suaˆˊt=Thể tıˊch CO₂ thực teˆˊThể tıˊch CO₂ lyˊ thuyeˆˊt×100Hiệu suaˆˊt=Thể tıˊch CO₂ lyˊ thuyeˆˊtThể tıˊch CO₂ thực teˆˊ×100Hiệu suaˆˊt=19.83222.4×100≈88.5%Hiệu suaˆˊt=22.419.832×100≈88.5%
Vậy hiệu suất của quá trình lên men là 88.5%.
Soˆˊ mol glucose=90180=0.5 molSoˆˊ mol glucose=18090=0.5mol
Soˆˊ mol CO₂=0.5×2=1 molSoˆˊ mol CO₂=0.5×2=1mol
�CO₂ lyˊ thuyeˆˊt=1×22.4=22.4 lıˊtVCO₂ lyˊ thuyeˆˊt=1×22.4=22.4lıˊt
B. Tính khối lượng các chất có trong dung dịch X:
Dung dịch X là dung dịch sau khi lên men rượu, trong đó có chứa ethanol (C₂H₅OH), một số sản phẩm phụ và nước.
Tổng khối lượng trước khi lên men là khối lượng glucose, tức là 90g. Sau quá trình lên men, ta thu được 23g ethanol và 44g CO₂. Phần còn lại sẽ là nước:
Khoˆˊi lượng nước=90−23−44=23 gKhoˆˊi lượng nước=90−23−44=23g
Tổng kết: