Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

* Phương pháp xác định nồng độ phần trăm dung dịch C u S O 4
- Cân một lượng dung dịch C u S O 4 xác định.
- Cô cạn dung dịch cho đến khi thu được chất rắn màu trắng đó là C u S O 4 . Sau đó đem cân lượng muối sau khi cô cạn này ta được số liệu là mct.
- Áp dụng công thức: 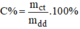 ta sẽ tính C% của dung dịch
C
u
S
O
4
.
ta sẽ tính C% của dung dịch
C
u
S
O
4
.
* Phương pháp xác định nồng độ mol của dung dịch C u S O 4 :
- Đong 1 thể tích dung dịch C u S O 4 xác định, đem cân lượng dung dịch đó.
- Sau đó dùng công thức 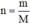 để tính số mol của
C
u
S
O
4
.
để tính số mol của
C
u
S
O
4
.
- Tính nồng độ mol của dung dịch
C
u
S
O
4
bằng công thức: 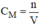

Bài 1: Bạn tự học nhé
Bài 2:
\(C_M=\dfrac{n}{V}=\dfrac{2,5}{4}=0,625M\)
Bài 3:
\(a,CuO+H_2\xrightarrow[]{t^o}Cu+H_2O\\ b,SO_3+H_2O\rightarrow H_2SO_4\)
Bài 4:
a, HNO3 - axit nitric
Ca(OH)2 - canxi hiđroxit
b, K2SO4
NaHCO3
mình làm nốt bài 1 :)))
oxit là 1 hợp chất trong đó có 1 hay nhiều nguyên tử Oxi liên kết với 1 đơn chất
VD : CO2 , FeO

trình bày phương pháp thực nghiệm để xác định nồng độ % và nồng độ mol của một mẫu thử dung dịch CuSO4
Trả lời
a) Phương pháp xác định nồng độ phần trăm của dung dịch CuSO4 .
– Cân lấy một lượng dung dịch CuSO4 tuỳ ý, ví dụ 100 g.
– Cô cạn dung dịch cho đến khi thu được chất rắn màu trắng là CuSO4.
– Cân muối CuSO4 thu được sau khi cô cạn, thí dụ được 8 g.
– Tính nồng độ phần trăm của dung dịch CuSO4 ban đầu :
C%=100%×8100=8%C%=100%×8100=8%
b) Phương pháp xác định nồng độ mol của dung dịch CuSO4 :
– Cân lấy một lượng dung dịch CuSO4 tuỳ ý rồi đo thể tích. Thí dụ, cân lấy 100 g dung dịch CuSO4 như trong thí nghiệm trên, đo thể tích được 90 ml.
– Tính số mol CuSO4 có trong 90 ml (hoặc 100 g) dung dịch là :
nCuSO4=8160=0,05(mol)nCuSO4=8160=0,05(mol)
– Tính nồng độ mol của dung dịch CuSO4 :
CM=1000×0,0590≈0,56(mol/l)
a) Phương pháp xác định nồng độ phần trăm của dung dịch CuSO4 .
– Cân lấy một lượng dung dịch CuSO4 tuỳ ý, ví dụ 100 g.
– Cô cạn dung dịch cho đến khi thu được chất rắn màu trắng là CuSO4.
– Cân muối CuSO4 thu được sau khi cô cạn, thí dụ được 8 g.
– Tính nồng độ phần trăm của dung dịch CuSO4 ban đầu :
C% = (100%×8):100=8%
b) Phương pháp xác định nồng độ mol của dung dịch CuSO4 :
– Cân lấy một lượng dung dịch CuSO4 tuỳ ý rồi đo thể tích. Thí dụ, cân lấy 100 g dung dịch CuSO4 như trong thí nghiệm trên, đo thể tích được 90 ml.
– Tính số mol CuSO4 có trong 90 ml (hoặc 100 g) dung dịch là :
\(_{n_{CuSO4}}\) = 8:160=0,05(mol)
– Tính nồng độ mol của dung dịch CuSO4 :
\(_{C_M}\)= (1000×0,05) : 90 ≈ 0,56(mol/l)

Đổi 500ml = 0,5l
\(C_{M\left(C\text{uS}O_4\right)}=\dfrac{n}{V_{\text{dd}}}=\dfrac{0,6}{0,5}=1,2M\)

\(n_{CuSO_4}=\dfrac{400}{160}=2,5\left(mol\right)\)
\(400ml=0,4\left(l\right)\)
\(C_{M_{CuSO_4}}=\dfrac{2,5}{0,4}=6,25\left(M\right)\)

Giải thích các bước giải:
a Để tính nồng độ % của dung dịch CuSO4 bão hòa ở nhiệt độ trên, ta dùng công thức:
Nồng độ % = (Khối lượng chất tan/Công thức phân tử chất tan) / Thể tích dung dịch x 100%
Với dung dịch CuSO4 bão hòa ở 60 độ C, ta có:
Khối lượng chất tan (CuSO4) = 40 kg = 40000 g
Thể tích dung dịch = 100 ml = 100 cm^3
Công thức phân tử CuSO4: 1 Cu + 1 S + 4 O = 63.5 + 32 + 4 x 16 = 159.5
Nồng độ % = (40000/159.5) / 100 = 25.08 %
Vậy, nồng độ % của dung dịch CuSO4 bão hòa ở nhiệt độ 60 độ C là khoảng 25.08 %.
b) Để tính khối lượng H2O cần dùng để pha vào dung dịch trên và có được dung dịch CuSO4 10%, ta dùng công thức:
Khối lượng H2O = Khối lượng chất tan ban đầu - Khối lượng chất tan sau pha / (Nồng độ sau pha - Nồng độ ban đầu)
Giả sử khối lượng chất tan sau khi pha là x g (= 10/100 x khối lượng dung dịch sau khi pha)
Vậy, ta có:
Khối lượng chất tan sau pha = 32 g + x g
Nồng độ sau pha = 10%
Nồng độ ban đầu = 25.08 %
Ứng dụng công thức, ta có:
x = (32 - 0.1 x (32 + x)) / (0.100 - 0.2508)
10000 x = 32 - 0.1 x (32 + x)
10000 x = 32 - 3.2 - 0.1x^2
0.1x^2 - 9967.2x + 3.2 = 0
Giải phương trình trên bằng phương pháp giải phương trình bậc hai ta có:
x ≈ 0.3145 hoặc x ≈ 9965.88
Với x ≈ 0.3145, ta được khối lượng H2O ≈ 32 - 0.3145 = 31.6855 g
Vậy, để có được dung dịch CuSO4 10%, ta cần dùng khoảng 31.6855 g nước.

$n_{Na_2CO_3} = n_{Na_2CO_3.10H_2O} = \dfrac{28,6}{286} = 0,1(mol)$
$C_{M_{Na_2CO_3}} = \dfrac{0,1}{0,2} = 0,5M$
$m_{dd} = D.V = 200.1,05 = 210(gam)$
$C\%_{Na_2CO_3} = \dfrac{0,1.106}{210}.100\% = 5,05\%$
Refer.
Phương pháp xác định nồng độ phần trăm của dung dịch CuSO4 .
– Cân lấy một lượng dung dịch CuSO4 tuỳ ý, ví dụ 100 g.
– Cô cạn dung dịch cho đến khi thu được chất rắn màu trắng là CuSO4.
– Cân muối CuSO4 thu được sau khi cô cạn, thí dụ được 8 g.
– Tính nồng độ phần trăm của dung dịch CuSO4 ban đầu :
\(C\%=\dfrac{8}{100}\cdot100\%=8\%\)
Phương pháp xác định nồng độ mol của dung dịch CuSO4 :
– Cân lấy một lượng dung dịch CuSO4 tuỳ ý rồi đo thể tích. Thí dụ, cân lấy 100 g dung dịch CuSO4 như trong thí nghiệm trên, đo thể tích được 90 ml.
– Tính số mol CuSO4 có trong 90 ml (hoặc 100 g) dung dịch là :
\(n_{CuSO_4}=\dfrac{8}{160}=0.05\left(mol\right)\)
– Tính nồng độ mol của dung dịch CuSO4 :
\(C_M=\dfrac{1000\cdot0.05}{90}=0.56\left(M\right)\)