Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Oxit cao nhất của nguyên tố R có dạng R2O5
\(\Rightarrow\) Hợp chất R với H ở thể khí có công thức là RH3
\(d_{RH_3/kk}=1,172\Rightarrow M_{RH_3}=1,172.29=34\left(đvC\right)\)
Ta có: \(M_{RH_3}=R+3=34\\ \Rightarrow R=31\)
Vậy R là Phốt pho (P)

Nguyên tố 'R' có oxit cao nhất là R2O3, => Hóa trị cao nhất của 'R' là 6
Hóa trị thấp nhất của R trong hợp chất với oxygen + Hóa trị của R trong hợp chất
thi với hydrogen = 8
=> Hóa trị của R trong hợp chất thi với hydrogen = 8 - 6 = 2
=> Công thức hợp chất thi với hydrogen là RH2
Ta có: %MH(R+H2) = (2/(R+2)) * 100
=> 5,88 = (2/(R+2)) * 100
=> R = 32
=> R là Sulfur (S)

a)
Do R thuộc nhóm VA
=> CTHH của R và H là: RH3
Có \(\dfrac{3}{M_R+3}.100\%=17,64\%=>M_R=14\left(g/mol\right)\)
=> R là N
b) Do CTHH của R và H là RH3
=> oxit cao nhất của R là R2O5
Có: \(\dfrac{16.5}{2.M_R+16.5}.100\%=74,07\%=>M_R=14\left(g/mol\right)\)
=> R là N

Đáp án B
Oxit cao nhất của một đơn chất X có dạng RO3.
⇒ Hợp chất khí với Hidro là H2R.
Ta có: 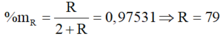
Vậy R là Se
