Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bài 4 câu a đề là thể tích H2 nha bạn
a)\(Fe2O3+3H2-->2Fe+3H2O\)
\(n_{Fe2O3}=\frac{12}{160}=0,075\left(mol\right)\)
\(n_{H2}=3n_{Fe2O3}=0,225\left(mol\right)\)
\(V_{H2}=0,225.22,4=5,04\left(l\right)\)
b)\(n_{Fe}=2n_{Fe2O3}=0,15\left(mol\right)\)
\(m_{Fe}=0,15.56=8,4\left(g\right)\)
Bài 6
a)\(Zn+H2SO4-->ZnSO4+H2\)
\(n_{Zn}=\frac{19,5}{65}=0,3\left(mol\right)\)
\(n_{ZnSO4}=n_{Zn}=0,3\left(mol\right)\)
\(m_{ZnSO4}=0,3.162=48,3\left(g\right)\)
b)\(n_{H2}=n_{Zn}=0,3\left(mol\right)\)
\(V_{H2}=0,3.22,4=6,72\left(l\right)\)

Bài I
1. Lập công thức hoá học của :
a) Nhôm(III) VÀ oxi: Al2O3
b) Natri và nhóm SO4: Na2SO4
c) Bari và nhóm OH: Ba(OH)2
2. Tính phân tử khối của NaOH và FeCl3
+) PTKNaOH = 23 + 16 + 1 = 40đvC
+) PTKFeCl3 = 56 + 3 x 35,5 = 162,5 đvC
Bài II:
1. Tính số mol của 11,2 gam sắt.
=> nFe = \(\frac{11,2}{56}=0,2\left(mol\right)\)
2. Tính số mol của 1,12 lít khí hiđro(đktc)
=> nH2 = \(\frac{1,12}{22,4}=0,05\left(mol\right)\)
3. Tìm khối lượng của 4,8 lít CO2 (đktc)
=> nCO2 = \(\frac{4,8}{22,4}=\frac{3}{14}\left(mol\right)\)
=> mCO2 = \(\frac{3}{14}.44=9,43\left(gam\right)\)
4. Tìm số mol của 11,1 gam CaCl2
=> ncaCl2 = \(\frac{11,1}{111}=0,1\left(mol\right)\)
Bài III
1. PTHH: Fe2O3 + 3H2 =(nhiệt)=> 2Fe + 3H2O
2. Ta có: nFe = \(\frac{16}{160}=0,1\left(mol\right)\)
a) Theo phương trình, nH2 = 0,1 x 3 = 0,3 (mol)
=> VH2(đktc) = \(0,3\times22,4=6,72\left(l\right)\)
b) Theo phương trình, nFe = 0,1 x 2 = 0,2 (mol)
=> mFe = 0,2 x 56 = 11,2 (gam)

nH2 = 2.24/22.4 = 0.1 (mol)
Fe + 2HCl => FeCl2 + H2
0.1...............................0.1
mFe = 0.1 * 56 = 5.6 (g)

FexOy+yCO\(\rightarrow\)xFe+yCO2(1)
CO2+Ca(OH)2\(\rightarrow\)CaCO3+H2O(2)
- Theo PTHH (2): \(n_{CO_2}=n_{CaCO_3}=\dfrac{7}{100}=0,07mol\)
- Theo PTHH(1) ta thấy: Ooxit+OCO=OCO2
\(\rightarrow\)nO(oxit)=nO(CO2)-nO(CO)=0,07.2-0,07=0,07 mol
mO(oxit)=0,07.16=1,12 gam
m=mFe=4,06-1,12=2,94 gam\(\rightarrow\)nFe=\(\dfrac{2,94}{56}=0,0525mol\)
\(\dfrac{x}{y}=\dfrac{n_{Fe}}{n_O}=\dfrac{0,0525}{0,07}=\dfrac{3}{4}\)
Fe3O4

Ta có: \(n_{H_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
a, PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
_____0,05__0,1____________0,05 (mol)
b, mFe = 0,05.56 = 2,8 (g)
c, mHCl = 0,1.36,5 = 3,65 (g)
\(\Rightarrow m_{ddHCl}=\dfrac{3,65}{10\%}=36,5\left(g\right)\)
Bạn tham khảo nhé!

a) Sơ đồ : CO + Fe2O3 ---> CO2 + Fe
PTHH : 6CO + 2Fe2O3 -> 6CO2 + 4Fe
b) Áp dụng định luật bảo toàn khối lượng ta có :
\(m_{CO}+m_{Fe_2O_3}=m_{CO_2}+m_{Fe}\)
c) Từ PTKL trên ta có :
8,4 + 16 = 13,2 + mFe
=> mFe = ( 8,4 + 16 ) - 13,2 = 11,2 ( g )

Câu 1 :
mAl = \(7,5\times\dfrac{36}{100}=2,7\left(g\right)\)
=> nAl = \(\dfrac{2,7}{27}=0,1\) mol
mMg = mhh - mAl = 7,5 - 2,7 = 4,8 (g)
=> nMg = \(\dfrac{4,8}{24}=0,2\) mol
Pt: 2Al + 6HCl --> 2AlCl3 + 3H2
0,1 mol------------> 0,1 mol-> 0,15 mol
.....Mg + 2HCl --> MgCl2 + H2
0,2 mol-----------> 0,2 mol-> 0,2 mol
mhh muối = mAlCl3 + mMgCl2 = (0,1 . 133,5) + (0,2 . 95) = 32,35 (g)
VH2 thu được = (0,15 + 0,2) . 22,4 = 7,84 (lít)
Câu 3 :
nZn = \(\dfrac{13}{65}=0,2\) mol
nHCl = \(\dfrac{21,9}{36,5}=0,6\) mol
Pt: Zn + 2HCl --> ZnCl2 + H2
0,2 mol-> 0,4 mol--------> 0,2 mol
Xét tỉ lệ mol giữa Zn và HCl:
\(\dfrac{0,2}{1}< \dfrac{0,6}{2}\)
Vậy HCl dư
mHCl dư = (0,6 - 0,4) . 36,5 = 7,3 (g)
VH2 thu được = 0,2 . 22,4 = 4,48 (lít)
Sau khi pứ kết thúc cho giấy quỳ tím vào quỳ tím chuyển sang màu đỏ vì HCl dư


Số mol
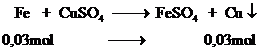
Phương trình
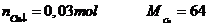
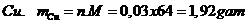
 khối lượng
khối lượng
Vậy khối lượng kim loại  là 1,92 gam
là 1,92 gam

Ta có: \(n_{H_2SO_4}=\dfrac{58,8}{98}=0,6\left(mol\right)\)
\(PTHH:2Al+3H_2SO_4--->Al_2\left(SO_4\right)_3+3H_2\uparrow\)
0,4 <--- 0,6 -----------> 0,2 --> 0,6
\(\Rightarrow\left\{{}\begin{matrix}m_{Al}=0,4.27=10,8\left(g\right)\\m_{Al_2\left(SO_4\right)_3}=0,2.342=68,4\left(g\right)\\V_{H_2}=0,6.22,4=13,44\left(lít\right)\end{matrix}\right.\)
Số hơi xấu ._. Mình thấy mình làm đúng rồi đó. Nhưng bạn cứ xem lại xem sao nhé!