Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Oxit axit :
$SO_3$cro : lưu huỳnh trioxit
$CO_2$ : cacbon đioxit
$CrO_3$ : Crom VI oxit
$SO_2$ : Lưu huỳnh đioxit
$P_2O_5$ : điphotpho pentaoxit
Oxit bazo :
$FeO$ : Sắt II oxit
$CaO$ : Canxi oxit
$K_2O$ : Kali oxit
$MgO$ : Magie oxit
Oxit lưỡng tính :
$ZnO$ : Kẽm oxit
$Al_2O_3$ : Nhôm oxit
Oxit trung tính
$N_2O$ : đinito oxit
$CO$ : cacbon oxit
$FeO + H_2SO_4 \to FeSO_4 +H_2O$
$CaO + H_2SO_4 \to CaSO_4 + H_2O$
$ZnO + H_2SO_4 \to ZnSO_4 + H_2O$
$K_2O + H_2SO_4 \to K_2SO_4 + H_2O$
$Al_2O_3 + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2o$
$MgO + H_2SO_4 \to MgSO_4 + H_2O$

a) $4P + 5O_2 \xrightarrow{t^o} 2P_2O_5$
b) $Mg + Cl_2 \xrightarrow{t^o} MgCl_2$
c) $2Na + 2H_2O \to 2NaOH + H_2$
d) $C + O_2 \xrightarrow{t^o} CO_2$
e) $C_xH_y + (x + \dfrac{y}{4})O_2 \xrightarrow{t^o} xCO_2 + \dfrac{y}{2}H_2O$
f) $2Al + Fe_2O_3 \xrightarrow{t^o} Al_2O_3 + 2Fe$
g) $2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2$
i) $Fe_xO_y + yCO \xrightarrow{t^o} xFe + yCO_2$
k) $Fe_2O_3 + 6HCl \to 2FeCl_3 +3 H_2O$
l) $3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4$

2.
a) 2Na + O2 -> 2NaO
b) P2O5 + 3H2O -> 2H3PO4
c) HgO -> Hg + 1/2O2
d) 2Fe(OH)3 -> Fe2O3 + 3H2O
e) Na2CO3 + CaCl2 -> CaCO3 + 2NaCl

\(a) 4K + O_2 \xrightarrow{t^o} 2K_2O\\ K_2O + H_2O \to 2KOH\\ 4P + 5O_2 \xrightarrow{t^o} 2P_2O_5\\ P_2O_5 + 3H_2O \to 2H_2PO_4\\ c) 2H_2 + O_2 \xrightarrow{t^o} 2H_2O\\ Na_2O + H_2O \to 2NaOH\\ d) 2Ca + O_2 \xrightarrow{t^o} 2CaO\\ CaO + H_2O \to Ca(OH)_2\\ e) 2Cu + O_2 \xrightarrow{t^o} 2CuO\\ CuO+ 2HCl\to CuCl_2 + H_2O\\ \)
\(b) S + O_2 \xrightarrow{t^o} SO_2 \\2SO_2 + O_2 \xrightarrow{t^o,V_2O_5} 2SO_3\\ SO_3 + H_2O \to H_2SO_4\)

1)
Trích mẫu thử
Sục mẫu thử vào dung dịch nước vôi trong :
- mẫu thử tạo vẩn đục trắng là $CO_2$
$CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O$
Nung nóng mẫu thử còn với Cu :
- mẫu thử làm chất chuyển từ màu nâu đỏ sang đen là $O_2$
$2Cu + O_2 \xrightarrow{t^o} 2CuO$
- mẫu thử không hiện tượng là $N_2$
Câu 2 :
Oxit là $CuO,SO_2,CO_2$
Câu 3 :
- Oxit bazo :
$Fe_2O_3$ : Sắt III oxit
$ZnO $: Kẽm oxit
$K_2O$ : Kali oxit
- Oxit axit :
$CO_2 $ : Cacbon đioxit
$SO_2$ : Lưu huỳnh đioxit
$P_2O_3$ : Điphotpho trioxit
$N_2O_5$ : Đinito pentaoxit
- Oxit trung tính :
$CO$ : Cacbon monooxit

\(2Al+6HCl\Rightarrow2AlCl_3+3H_2\\ Mg+2HNO_3\Rightarrow Mg\left(NO_3\right)_2+H_2\\ C_2H_6O+3O_2\underrightarrow{t^o}2CO_2+3H_2O\\ 4P+5O_2\Rightarrow2P_2O_5\)
2Al(OH)3 → Al2O3 + 3H2O
Fe3O4 + 2C → 3Fe + 2CO2

Bài 1.
| CTHH | Tên | Phân loại |
| BaO | Bari oxit | oxit |
| Fe2O3 | Sắt (III) oxit | oxit |
| MgCl2 | Magie clorua | muối |
| NaHSO4 | Matri hiđrosunfat | muối |
| Cu(OH)2 | Đồng (II) hiđroxit | bazơ |
| SO3 | Lưu huỳnh trioxit | oxit |
| Ca3(PO4)2 | Canxi photphat | muối |
| Fe(OH)2 | Sắt (II) hiđroxit | bazơ |
| Zn(NO3)2 | Kẽm nitrat | muối |
| P2O5 | điphotpho pentaoxit | oxit |
Bài 2.
a.Trích một ít mẫu thử và đánh dấu
Đưa quỳ tím vào 3 dd:
-NaOH: quỳ hóa xanh
-H2SO4: quỳ hóa đỏ
-Na2SO4: quỳ không chuyển màu
b.Trích một ít mẫu thử và đánh dấu
Đưa nước có quỳ tím vào 3 chất:
-Na2O: quỳ hóa xanh
-P2O5: quỳ hóa đỏ
-MgO: quỳ không chuyển màu
Bài 3.
a.\(Fe_2O_3+3H_2\rightarrow\left(t^o\right)2Fe+3H_2O\)
b.\(SO_3+H_2O\rightarrow H_2SO_4\)
c.\(4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\)
d.\(Ca+2H_2O\rightarrow Ca\left(OH\right)_2+H_2\)
e.\(2K+2H_2O\rightarrow2KOH+H_2\)
Bài 1:
BaO: oxit bazơ - Bari oxit.
Fe2O3: oxit bazơ - Sắt (III) oxit.
MgCl2: muối trung hòa - Magie clorua.
NaHSO4: muối axit - Natri hiđrosunfat.
Cu(OH)2: bazơ - Đồng (II) hiđroxit.
SO3: oxit axit - Lưu huỳnh trioxit.
Ca3(PO4)2: muối trung hòa - Canxi photphat.
Fe(OH)2: bazơ - Sắt (II) hiđroxit.
Zn(NO3)2: muối trung hòa - Kẽm nitrat.
P2O5: oxit axit - Điphotpho pentaoxit.
Bạn tham khảo nhé!

Phản ứng: a, b, c, d
\(a\text{)}2CO+O_2\underrightarrow{t^o}2CO_2\)
- Chất oxi hoá: O2, CO
- Chất khử: CO
\(b\text{)}2Al+Fe_2O_3\underrightarrow{t^o}Al_2O_3+2Fe\)
- Chất oxi hoá: Fe2O3
- Chất khử: Al
\(c\text{)}Mg+CO_2\underrightarrow{t^o}MgO+CO\)
- Chất oxit hoá: CO2
- Chất khử: Mg
\(d\text{)}CO+H_2O\underrightarrow{t^o}CO_2\uparrow+H_2\uparrow\)
- Chất oxi hoá: H2O, CO
- Chất khử: CO
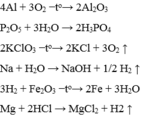
1.
\(a.2K+2H_2O\rightarrow2KOH+H_2\uparrow\)
\(b.3Ca\left(OH\right)_2+2H_3PO_4\rightarrow Ca_3\left(PO_4\right)_2+6H_2O\)
\(c.4FeS_2+11O_2\underrightarrow{t^o}2Fe_2O_3+8SO_2\)
\(d.Fe_xO_y+\left(y-x\right)CO\rightarrow xFeO+\left(y-x\right)CO_2\)
2.
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
\(2Cu+O_2\underrightarrow{t^o}2CuO\)
\(S+O_2\underrightarrow{t^o}SO_2\)
\(C+O_2\underrightarrow{t^o}CO_2\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
\(2Mg+O_2\underrightarrow{t^o}2MgO\)
\(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
\(4K+O_2\underrightarrow{t^o}2K_2O\)
Câu 3:
Lấy mẫu thử và đánh dấu từng mẫu thử
Hòa tan các mẫu thử vào nước
Na + H2O => NaOH + 1/2 H2
P2O5 + 3H2O => 2H3PO4
CaO + H2O => Ca(OH)2
Chất tan trong nước là: Na, P2O5, CaO, NaCl (muối ăn tan trong nước tạo thành nước muối)
Chất tan trong nước và sau phản ứng có khí thoát ra là Na => nhận biết được Na
Chất rắn không tan: Mg + Ag
Cho dung dịch HCl vào 2 mẫu thử chất rắn không tan
Mg + 2HCl => MgCl2 + H2
Mẫu thử nào tan trong HCl và có khí thoát ra là Mg
Mẫu thử không có hiện tượng gì là Ag (vì Ag không tác dụng với dung dịch HCl)
Cho quỳ tím vào các mẫu thử tan trong nước
Mẫu thử nào làm quỳ tím hóa đỏ => chất ban đầu là P2O5
Mẫu thử nào làm quỳ tím hóa xanh => chất ban đầu là CaO
Mẫu thử nào quỳ tìm không đổi màu => chất ban đầu là NaCl