Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Phương trình hóa học: M O + 2 H C l → M C l 2 + H 2 O
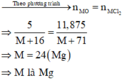

gọi M là ct của kim loại đó
ta có ptpư:
2 M + xCl2 >>>2 MClx
2M g 2 M + 71x g
3,6g 14,25g
ta có: 28,5M=7,2M + 255,6x
21,3M =255,6x
M=255,6x/21,3
nếu x=1>>>M=12(loại vì đó là fi kim)
x=2>>>M=24(nhận vì là kim loại)
>>> M là Mg

số mol hí thu được là:\(n_{H_2}=\frac{V_{H_2}}{22,4}=\frac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: \(X+H_2SO_4\rightarrow XSO_4+H_2\)
0,2 0,2 (mol)
\(M_X=\frac{m}{n}=\frac{13}{0,2}=65\left(đvC\right)\)
→kim loại hóa trị II có M=65 là kẽm (Zn)
X+H2SO4\(\rightarrow\) XSO4+H2
n của h2 =0,2 mol\(\Rightarrow\) n của X=0.2 \(\Rightarrow\) Mcủa X=13:0,2=....
tra bảng tuần hoàn là ra x

Đáp án B.
Gọi kim loại là R.
Bảo toàn khối lượng:
mO = 16,2 - 13 = 3,2
=> nO2= 0,1 (mol)
2R + O2→ 2RO
0,2 0,1
MR = 65(Zn)
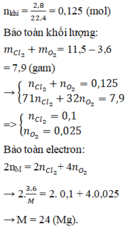
2R+O2->2RO
Theo PTHH, ta có: nR=nRO
\(\Rightarrow\)\(\dfrac{3,6}{R}\)=\(\dfrac{6}{R+16}\)
\(\Rightarrow\) R = 24 (Mg)
Đáp án C. Mg
C.Mg