Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
![]()
=> Y chứa H + dư
![]()
![]()
Bảo toàn khối lượng:
![]()
![]()
![]()
Bảo toàn nguyên tố Hidro: n N H 4 + = 0 , 04 m o l
Bảo toàn nguyên tố Nito: n F e ( N O 3 ) 2 = 0 , 08 m o l
![]()
![]()
![]()
![]()
Bảo toàn e:
![]()
![]()
![]()
Bảo toàn nguyên tố Clo:
![]()
![]()
= 298,31 (g)
Giải hệ => x = 0,52 mol; y = 0,12 mol ![]()

Đáp án B
Thêm AgNO3 vào Y → NO chứng tỏ trong Y có chứa cặp H+ và Fe2+ → anion trong Y chỉ có Cl- mà thôi.
Lượng H+ dư được tính nhanh = 4nNO = 0,18 mol → lượng phản ứng là 1,64 mol.
Sơ đồ:
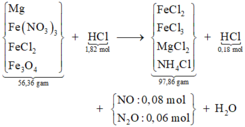
Bảo toàn khối lượng cả sơ đồ có
![]()
Theo đó, bảo toàn nguyên tố H có 0,04 mol NH4Cl và có 0,08 mol Fe(NO3)3 (theo bảo toàn N sau đó).
Tiếp tục theo bảo toàn electron mở rộng hoặc dùng bảo toàn O có ngay số mol Fe3O4 là 0,04 mol.
Gọi số mol Mg và FeCl2 trong X lần lượt là x, y mol → 24x + 127y = 27,72 gam.
Xét toàn bộ quá trình, bảo toàn electron ta có:


Đáp án B
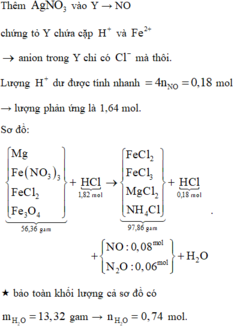
Theo đó, bảo toàn nguyên tố H có 0,04 mol NH4Cl và có 0,08 mol Fe(NO3)3 (theo bảo toàn N sau đó).
Tiếp tục theo bảo toàn electron mở rộng hoặc dùng bảo toàn O có ngay số mol Fe3O4 là 0,04 mol.
« Gọi số mol Mg và FeCl2 trong X lần lượt là x, y mol


Đặt a, b, c là số mol Al203, CuO , FeO mA = 102a + 80b + 72c = 20,3 m rắn = 102a + 64b + 56c = 17,1 nHCl = 6a + 2b + 2c = 0,7 -> a = 0,05 ; b = c = 0,1 Trong B chứa nCO2 = b + c = 0,2 nCaCO3 = 0,1 -> nCa(HCO3)2 = 0,05 -> nCa(OH)2 = 0,15 -> Vdd =105 ml

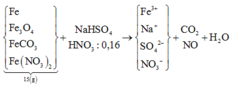
Ta có m rắn là Fe203 n Fe=0,09
Bảo toàn nguyên tố N
có nN(trong axit) = nN(trongNO3- muối) + nN(trongNO) = 3x + 0,09*3 + 0,11 n Al=x=0,1
Vì là oxit sắt nên có thể là FeO, Fe2O3 hoặc Fe3O4
Fe2O3 thì loại.mà FeO hay Fe304 khi lên Fe3+ đều nhường 1e 3x + y =0,11*3 suy ra x=0,03 =1/3 n Fe vậy ct sắt là Fe304
m=0,1*27+0,03*232=9,66




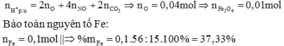
A. 184,1 gam và 91,8 gam.
B. 84,9 gam và 91,8 gam.
C. 184,1 gam và 177,9 gam.
D. 84,9 gam và 86,1 gam.