Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Các oxit tác dụng với nước: N a 2 O , P 2 O 5 , C O 2 , S O 3
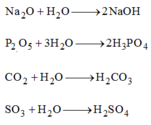
- Các oxit không hòa tan trong nước: CuO, MgO, A l 2 O 3 .

Dung dịch sau phản ứng làm biến đổi giấ quỳ hóa xanh vì sau phản ứng thu được dung dịch bazo ( NaOH, KOH).

SO2 + 2NaOH → Na2SO3 + H2O
\(n_{SO_2}=\frac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{NaOH}=0,5\times2,5=1,25\left(mol\right)\)
a) Theo pT: \(n_{SO_2}=\frac{1}{2}n_{NaOH}\)
Theo bài: \(n_{SO_2}=\frac{6}{25}n_{NaOH}\)
Vì \(\frac{6}{25}< \frac{1}{2}\) ⇒ NaOH dư
Theo pT: \(n_{NaOH}pư=2n_{SO_2}=2\times0,3=0,6\left(mol\right)\)
\(\Rightarrow n_{NaOH}dư=1,25-0,6=0,65\left(mol\right)\)
\(\Rightarrow m_{NaOH}dư=0,65\times40=26\left(g\right)\)
b) DD sau pứ: NaOH dư và Na2SO3
\(C_{M_{NaOH}}dư=\frac{0,65}{0,5}=1,3\left(M\right)\)
Theo pT: \(n_{Na_2SO_3}=n_{SO_2}=0,3\left(mol\right)\)
\(\Rightarrow C_{M_{Na_2SO_3}}=\frac{0,3}{0,5}=0,6\left(M\right)\)

Câu 1)
a) 2HgO\(-t^0\rightarrow2Hg+O_2\)
b)Theo gt: \(n_{HgO}=\frac{2,17}{96}\approx0,023\left(mol\right)\\ \)
theo PTHH : \(n_{O2}=\frac{1}{2}n_{HgO}=\frac{1}{2}\cdot0,023=0,0115\left(mol\right)\\ \Rightarrow m_{O2}=0,0115\cdot32=0,368\left(g\right)\)
c)theo gt:\(n_{HgO}=0,5\left(mol\right)\)
theo PTHH : \(n_{Hg}=n_{HgO}=0,5\left(mol\right)\\ \Rightarrow m_{Hg}=0,5\cdot80=40\left(g\right)\)
Câu 2)
a)PTHH : \(S+O_2-t^0\rightarrow SO_2\)
b)theo gt: \(n_{SO2}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
theo PTHH \(n_S=n_{SO2}=0,1\left(mol\right)\\ \Rightarrow m_S=0,1\cdot32=3,2\left(g\right)\)
Ta có khối lượng S tham gia là 3,25 g , khối lượng S phản ứng là 3,2 g
Độ tinh khiết của mẫu lưu huỳnh là \(\frac{3,2}{3,25}\cdot100\%\approx98,4\%\)
c)the PTHH \(n_{O2}=n_{SO2}=0,1\left(mol\right)\Rightarrow m_{O2}=0,1\cdot32=3,2\left(g\right)\)

1/ chất tham gia : BaCl2, Na2SO4 sản phẩm tạo thành : BaSO4, NaCl
Sau phản ứng tổng kl của các chất tham gia phản ứng không đổi.
trước phản ứng 2 1 A B
2 1 A B Sau phản ứng thuyết trình thí nghiệm SGK trang 53![]()

Ta có phương trình hóa học :
BaCl2 + Na2SO4 → 2NaCl + BaSO4\(\uparrow\)
1. Những chất tham gia : BaCl2 và Na2SO4
Những chất sản phẩm : NaCl và BaSO4
Tổng khối lượng của các chất tham gia phản ứng và các chất sau phản ứng không thay đổi.
2. Tự làm
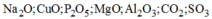

Dung dịch sau phản ứng làm quỳ tím hóa xanh: NaOH.
Dung dịch sau phản ứng làm quỳ tím hóa đỏ: H 3 P O 4 , H 2 C O 3 , H 2 S O 4