Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)
\(4FeCO_3 + O_2 \xrightarrow{t^o} 2Fe_2O_3 + 4CO_2\\ 4FeS_2 + 11O_2 \xrightarrow{t^o} 2Fe_2O_3 + 8SO_2\\ SO_2 + Br_2 + 2H_2O \to 2HBr + H_2SO_4\\ Fe_2O_3 + 3H_2SO_4 \to Fe_2(SO_4)_3 + 3H_2O\)
\(n_{FeCO_3} = a ; n_{FeS_2} = b \Rightarrow 116a + 120b = 35,2(1)\\ n_{khí} = n_{CO_2} + n_{SO_2} = a + 2b = \dfrac{8,96}{22,4} = 0,4(2)\\ (1)(2)\Rightarrow a = 0,2 ; b = 0,1\\ \%m_{FeCO_3} = \dfrac{0,2.116}{35,2} .100\% =65,91\%\\ \%m_{Fe_2O_3} = 100\% - 65,91\% = 34,09\%\)
b) Không có chất rắn nào còn lại trong dung dịch Z

\(\left\{{}\begin{matrix}FeS_2:x\left(mol\right)\\Cu_2S:y\left(mol\right)\end{matrix}\right.\)
4FeS2 + 11O2 \(\xrightarrow{t^o}\) 2Fe2O3 + 8SO2
x..............................0,5x.........2x...................(mol)
Cu2S + 2O2 \(\xrightarrow{t^o}\) 2CuO + SO2
y..........................2y...........y.............................(mol)
Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O
0,5x...........1,5x..................................................(mol)
CuO + H2SO4 → CuSO4 + H2O
2y............2y.................................................(mol)
Suy ra: 1,5x + 2y = 0,2.2,5(1)
SO2 + 2NaOH → Na2SO3 + H2O
(2x+y).....(4x+2y).........................................(mol)
Suy ra : 4x + 2y = 0,25.4(2)
Từ (1)(2) suy ra x = 0,2 ; y = 0,1
Vậy :
\(\%m_{FeS_2} = \dfrac{0,2.120}{0,2.120+0,1.160}.100\% = 60\%\\ \%m_{Cu_2S} = 100\% -60\% = 40\%\)

Đáp án C
Phương pháp: Gọi công thức chung 2 bazo là MOH (M = 101/3) với nMOH = 0,15
- Giả sử tạo các muối
+ Nếu chỉ tạo muối dạng MH2PO4
+ Nếu chỉ tạo muối dạng M2HPO4:
+ Nếu chỉ tạo muối M3PO4:
Để biết được hỗn hợp rắn gồm những chất nào, bảo toàn nguyên tố, bảo toàn khối lượng muối => đáp án
Hướng dẫn giải:
NaOH: 0,05
KOH: 0,1
Gọi công thức chung 2 bazo là MOH (M=101/3) với nMOH=0,15
- Nếu chỉ tạo muối dạng MH2PO4:
![]()
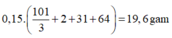
- Nếu chỉ tạo muối dạng M2HPO4:
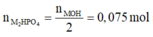
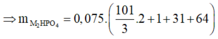
= 12,25 gam
- Nếu chỉ tạo muối dạng M3PO4:
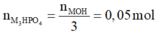
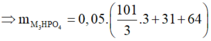
= 9,8 gam
Ta thấy mmuối < 9,8 gam => MOH dư, H3PO4 hết
Giả sử chất rắn gồm:
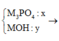
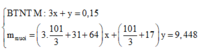
![]()
![]()
=> m = 1,302 gam

Đáp án B
nFeS2 = nAg2S =1/3 nSO2 = 0,055 mol
Chất rắn B gồm có Fe2O3 và Ag, cho qua H2SO4 thì chỉ còn lại Ag
⇒m=0,055 . 2 .108 = 11,88
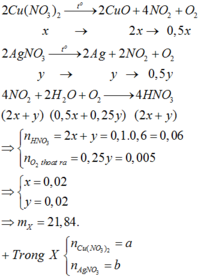
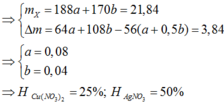
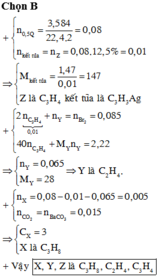

\(4FeS_2+11O_2\underrightarrow{t^0}2Fe_2O_3+8SO_2\)
\(Ag_2S+O_2\underrightarrow{t^0}2Ag+SO_2\)
\(A:Fe_2O_3,Ag\)
\(SO_2+Br_2+H_2O\rightarrow H_2SO_4+2HBr\)
\(B:H_2SO_4,HBr\)
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2\)
\(Fe_2O_3+6HBr\rightarrow2FeBr_3+3H_2O\)