Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Lời giải.
Lấy từ mỗi lọ một mẫu hóa chất (gọi là mẫu thử) để làm thí nghiệm nhận biết.
Cho quỳ tím vào mẫu thử từng chất và quan sát, thấy:
- Những dung dịch làm quỳ tím đổi màu là: NaOH và Ba(OH)2, (nhóm 1).
- Những dung dịch không làm quỳ tím đổi màu là: NaCl, Na2SO4 (nhóm 2).
Để nhận ra từng chất trong mỗi nhóm, ta lấy một chất ở nhóm (1), lần lượt cho vào mỗi chất ở nhóm (2), nếu có kết tủa xuất hiện thì chất lấy ở nhóm (1) là Ba(OH)2 và chất ở nhóm (2) là Na2SO4. Từ đó nhận ra chất còn lại ở mỗi nhóm.
Phương trình phản ứng: Ba(OH)2 + Na2SO4 → BaSO4 + NaOH
Quỳ tím hóa xanh Ba(OH)2 và NaOH
Cho 2 dung dịch hóa xanh thử vào từng lọ còn lại . làm kết tủa trắng là Na2SO4 và BaSO4
Còn lại là NaCl

bài 1:
- Trích mỗi chất 1 ít làm mẫu thử
- Nhỏ vài giọt các dd trên vào mẫu giấy quỳ tím
+ quỳ tím chuyển sang xanh : Ba(OH)2 , NaOH (I)
+ Không có hiện tượng gì : NaCl , Na2SO4 (II)
- Trích từng chất dd ở nhóm I vào nhóm II , thấy xuất hiện kết tủa trắng thì đó là Ba(OH)2 và Na2SO4
Ba(OH)2 + Na2SO4 → BaSO4↓ + 2NaOH
- Hai dd còn lại là NaCl(không làm quỳ tím đổi màu)
Và NaOH ( quỳ làm tím hóa xanh )

Có 5 lọ: Na2SO4, (CH3COO)2Ba, Al2(SO4)3, NaOH và Ba(OH)2
Rót từ từ các chất từ lọ này vào lọ khác ta có bảng sau:

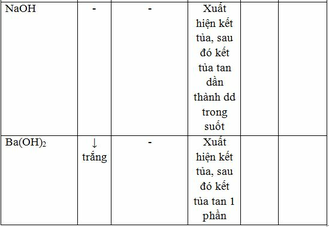
Dấu ‘ – ‘ thể hiện không có phản ứng xảy ra.
Từ giả thiết bài toán:
- Rót dung dịch từ lọ (4) vào lọ (3) hoặc (5) đều tạo kết tủa => lọ (4) có thể là Na2SO4 hoặc (CH3COO)2Ba vì từ bảng ta thấy 2 chất này cùng tạo 2 kết tủa với các chất khác.
- Rót từ từ đến dư dd trong lọ (2) vào lọ (1) thì có kết tủa sau đó kết tủa tan dần tạo thành dung dịch trong suốt => lọ (2) là NaOH; lọ (1) là Al2(SO4)3
- Rót từ từ đến dư dd lọ (5) vào lọ (1) thì có kết tủa sau đó kết tủa tan một phần => lọ (5) là Ba(OH)2 và lọ (1) là Al2(SO4)3.
- Từ lọ (5) là Ba(OH)2 => lọ (4) là Na2SO4 => lọ (3) là (CH3COO)2Ba
Kết luận: Vậy thứ tự các lọ là:
(1) Al2(SO4)3
(2) NaOH
(3) (CH3COO)2Ba
(4) Na2SO4
(5) Ba(OH)2
Các phản ứng hóa học xảy ra:
Na2SO4 + (CH3COO)2Ba → BaSO4↓ + 2CH3COONa
Na2SO4 + Ba(OH)2 → BaSO4↓ + 2NaOH
6NaOH + Al2(SO4)3 → 2Al(OH)3↓ + 3Na2SO4
NaOH dư + Al(OH)3↓ → NaAlO2 + 2H2O
Ba(OH)2 + Al2(SO4)3 → 2Al(OH)3↓ + 3BaSO4↓ (không tan khi cho Ba(OH)2 dư)
Ba(OH)2 + 2Al(OH)3↓ → Ba(AlO2)2 + 4H2O

1.
Cho dd HCl vào các dd trên nhận ra;
-Xuất hiện kết tủa trắng là AgNO3
-Xuất hiện khí ko màu là Na2CO3
-BaCl2; NaCl ko có hiện tượng
Cho dd H2SO4 vào 2 dd còn lại nhận ra:
-Xuất hiện kết tủa trắng là BaCl2
-NaCl ko có hiện tượng.
1.
- Trích mẫu thử vào các ống nghiệm và đánh số tương ứng sau đó nhỏ vài giọt dung dịch HCl vào các ống nghiệm:
+ Ống nào có sủi bọt khí → Na2CO3
+ Ống có kết tủa trắng → AgNO3
+ Không hiện tượng → BaCl2, NaCl
- Trích mẫu thử của 2 chất còn lại vào các ống nghiệm mới sau đó nhỏ vài giọt dung dịch H2SO4 vào:
+ Ống có kết tủa trắng → BaCl2
+ Không hiện tượng → NaCl
Các PTHH:
Na2CO3 + 2HCl → 2NaCl + H2O + CO2 ↑
AgNO3 + HCl → AgCl ↓ + HNO3
BaCl2 + H2SO4 → BaSO4 ↓ + 2HCl
2.
Lấy mỗi chất 1 ít cho ra các ổng nghiệm khác nhau và đánh dấu thứ tự
- Cho dung dịch NaOH lần lượt vào mỗi ống nghiệm
+ Xuất hiện kết tủa trắng là MgCl2
MgCl2 + 2NaOH \(\rightarrow\) Ma(OH)2\(\downarrow\) + NaCl
+Xuất hiện kết tủa nâu đỏ là Fe2(SO4)3
Fe2(SO4)3 + 6NaOH \(\rightarrow\) 3Na2SO4 + 2Fe(OH)3\(\downarrow\)
+Không có hiện tượng gì là Na2SO4 và NaCl(*)
-Cho dung dịch BaCl2 vào (*)
+Xuất hiện kết tủa trắng là Na2SO4
Na2SO4 + BaCl2 \(\rightarrow\) BaSO4 + 2NaCl
Còn lại NaCl không có hiện tượng g

Lấy mẫu các dung dịch rồi tiến hành đun nóng
- Xuất hiện kết tủa trắng, có bọt khí => Mg(HCO3)2 hoặc Ba(HCO3)2 (nhóm I)
\(\text{Mg(HCO3)2 to→ MgCO3↓ + H2O + CO2↑}\)
\(\text{Ba(HCO3)2 to→ BaCO3↓ + H2O + CO2↑}\)
- Xuất hiện bọt khí => KHCO3
\(\text{2KHCO3 to→ K2CO3↓ + H2O + CO2↑}\)
- Ko xảy ra hiện tượng gì => NaHSO4 hoặc Na2CO3 (nhóm II)
Làn lượt cho các chất ở nhóm I tác dụng với nhóm II
| Ba(HCO3)2 | Mg(HCO3)2 | |
| NaHSO4 | \(\downarrow\)trắng\(\uparrow\) | \(\uparrow\)trắng |
| Na2CO3 | \(\downarrow\)trắng | \(\downarrow\)trắng |
Ở thí nghiệm vừa tạo kết tủa và khí => chất ở nhóm I là Ba(HCO3)2, chất ở nhóm II là NaHSO4
\(\text{Ba(HCO3)2 + NaHSO4 -> BaSO4↓ + CO2↑ + H2O + Na2CO3}\)
buithianhtho, Pham Van Tien, Duong Le, Nguyễn Thị Kiều, Dương Chung, Linh, Luân Trần, Arakawa Whiter, Trần Quốc Toàn, Đặng Anh Huy 20141919, Nguyễn Nhật Anh, Trần Hữu Tuyển, Phùng Hà Châu, Quang Nhân, Hoàng Tuấn Đăng, Nguyễn Trần Thành Đạt, Nguyễn Thị Minh Thương , Nguyễn Anh Thư,...

cho chất p.p vào thì
chuyển sang màu hồng là;HCl, H2SO4
màu xanh: BaCl2,NaOH, Ba2SO4
ta kẻ bảng cho hai nhóm trên lần lượt tác dụng với nhau là ra

- Trích lần lượt các chất ra ống thử
- Cho dung dịch AgNO3 vào từng mẫu thử mẫu nào xuất hiện kết tủa trắng là HCl và NaCl
HCl + AgNO3 \(\rightarrow\) AgCl\(\downarrow\) + HNO3
NaCl + AgNO3 \(\rightarrow\) AgCl\(\downarrow\) + NaNO3
- Sau đó ta chia bốn dung dịch đó làm hai nhóm
+ Nhóm 1 : HCl ; NaCl
+ Nhóm 2 : H2SO4 ; Na2SO4
- Sau đó cho quỳ tím vào hai nhóm
+ Ở nhóm 1 : mẫu thử nào làm quỳ tím hóa đỏ là HCl còn lại là NaCl
+ Ở nhóm 2 : mẫu thử nào làm quỳ tím hóa đỏ là H2SO4 còn lại là Na2SO4
Cho 5,8Mg(OH)2,tác dụng với dung dịch H2sO4 một lượng vừa và đủ.tính khối lượng muối thu được
Tính Mg=24,S=32,O=16,H=1

Trích các mẫu thử
Cho dd NaOH vào các mẫu thử nhận ra:
+AgNO3 kết tủa màu đen
+CuSO4 kết tủa màu xanh
+NaCl ko PƯ