Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Biểu thức tốc độ tức thời của phản ứng là:
v1 = k.CCl2.CH2
b) Gọi CCl2 là nồng độ ban đầu của Cl, CH2 là nồng độ đầu của H2
=> v2 = k. CCl2.CH2 :2
=> 2v2 = v1
=> Tốc độ phản ứng giảm 1 nửa khi nồng độ H2 giảm 2 lần và giữ nguyên nồng độ Cl2

Áp suất tăng 2 lần thì thể tích giảm 2 lần nên nồng độ tăng 2 lần và phản ứng xảy ra chiều thuận. Do đó tốc độ phản ứng sẽ tăng 2.2 = 4 lần.
Áp suất tăng 2 lần thì thể tích giảm 2 lần nên nồng độ tăng 2 lần và phản ứng xảy ra chiều thuận. Do đó tốc độ phản ứng sẽ tăng 2.2 = 4 lần.

Áp suất tăng 2 lần thì thể tích giảm 2 lần nên nồng độ tăng 2 lần và phản ứng xảy ra chiều thuận. Do đó tốc độ phản ứng sẽ tăng 2.2 = 4 lần.
Áp suất tăng 2 lần thì thể tích giảm 2 lần nên nồng độ tăng 2 lần và phản ứng xảy ra chiều thuận. Do đó tốc độ phản ứng sẽ tăng 2.2 = 4 lần.

Áp suất tăng 2 lần thì thể tích giảm 2 lần nên nồng độ tăng 2 lần và phản ứng xảy ra chiều thuận. Do đó tốc độ phản ứng sẽ tăng 2.2 = 4 lần.

Gọi ∆CNO, ∆CH2, ∆CN2, ∆CH2O lần lượt là biến thiên nồng độ các chất NO, H2, N2 và H2O trong khoảng thời gian . Tốc độ trung bình của phản ứng được tính theo biểu thức: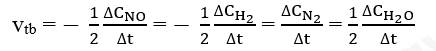

- Trong phản ứng hóa học có sự tham gia của chất khí, áp xuất sẽ ảnh hưởng đến tốc độ phản ứng
=> Yếu tố áp suất ảnh hưởng đến tốc độ phản ứng (1)
- Khi tăng áp suất, tốc độ phản ứng tăng
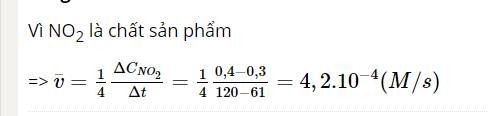
a) Công thức tính tốc độ tức thời của phản ứng là: v1 = k.CNO2.CO2
b)
- Nồng độ O2 tăng 3 lần, nồng độ NO không đổi: v2 = k.CNO2.(CO2.3)
=> v2 tăng 3 lần so với v1
- Nồng độ NO tăng 3 lần, nồng độ O2 không đổi: v3 = k.(CNO.3)2.CO2 = k.CNO2.9.CO2
=> v3 tăng 9 lần so với v1
- Nồng độ NO và O2 đều tăng 3 lần: v4 = k.(CNO.3)2.(CO2.3) = k.CNO2.27.CO2
=> v4 tăng 27 lần so với v1