Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1)
$n_{P_2O_5} = 0,05(mol) \Rightarrow n_{H_3PO_4} = 0,05.2 = 0,1(mol)$
$n_{KOH} = 0,2(mol) = 2n_{H_3PO_4}$. Suy ra : muối là $K_2HPO_4$
$n_{K_2HPO_4} = n_{H_3PO_4} = 0,1(mol)$
$m_{muối} = 0,1.174 = 17,4(gam)$
2)
$n_{H_3PO_4} = 2n_{P_2O_5} = 0,2(mol)$
$1 < n_{KOH} : n_{H_3PO_4} = 0,35 : 0,2 = 1,75 < 2$ nên muối gồm $KH_2PO_4$ và $K_2HPO_4$

nKOH = 0,1.1,5 = 0,15 mol , nH3PO4 = 0,2.0,5 = 0,1 mol
T = \(\dfrac{nKOH}{nH_3PO_4}\)= \(\dfrac{0,15}{0,1}\)= 1,5 => tạo 2 muối \(\left\{{}\begin{matrix}H_2PO_4^-\\HPO_4^{2-}\end{matrix}\right.\)
KOH + H3PO4 ---> KH2PO4 + H2O
2KOH + H3PO4 ---> K2HPO4 + 2H2O
Gọi số mol KH2PO4 và K2HPO4 lần lượt là x và y , theo tỉ lệ phản ứng ta có
\(\left\{{}\begin{matrix}x+y=0,1\\x+2y=0,15\end{matrix}\right.\)=> x = 0,05 và y = 0,05
mKH2PO4 = 0,05. 136 = 6,8 gam , mK2HPO4 = 0,05 . 174 = 8,7 gam.

Đáp án B
Hướng dẫn giải:
P2O5+ 3H2O → 2 H3PO4
0,11 0,22mol
NaOH + H3PO4 → NaH2PO4 + H2O
2NaOH + H3PO4 → Na2HPO4 + 2H2O
3NaOH + H3PO4 → Na3PO4 + 3H2O
Nếu chất tan trong dung dịch chỉ chứa các muối thì:
Theo các PT ta có: nH2O= nNaOH= 0,4a (mol)
Áp dụng định luật bảo toàn khối lượng ta có:
mNaOH + mH3PO4= mmuối + mH2O →0,4a. 40 + 0,22.98= 24,2 + 0,4a.18 → a= 0,3 M
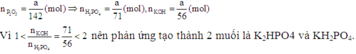
\(n_{P_2O_5}=\dfrac{71}{142}=0,5\left(mol\right);n_{KOH}=0,2.2=0,4\left(mol\right)\)
PTHH: P2O5 + 6KOH → 2K3PO4 + 3H2O
Mol: 0,07 0,4 0,13
Ta có:\(\dfrac{0,5}{1}>\dfrac{0,4}{6}\)⇒ KHO pứ hết;P2O5 dư
\(\Rightarrow m_{P_2O_5dư}=\left(0,5-0,07\right).142=61,06\left(g\right)\)
\(m_{K_3PO_4}=0,13.212=27,56\left(g\right)\)