Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
2 :6 :2 :3
0.3 \(\rightarrow0,45\)
\(n_{Ạl}=\dfrac{8.1}{27}=0.3\left(mol\right)\)
\(\Rightarrow\)\(n_{H_2}=0.459\left(mol\right)\) \(\Rightarrow V_{H_2}=0,45.22,4=10,08\left(l\right)\)
\(3H_2+Fe_2O_3\rightarrow2Fe+3H_2O\)
3 :1 :2 ;3
0,45 \(\rightarrow0,3\left(mol\right)\)
\(\Rightarrow n_{Fe}=0,3\left(mol\right)\)
\(\Rightarrow m_{Fe}=0,3.56=16,8\left(g\right)\)
\(\Rightarrow H=\dfrac{11,2}{16,8}.100=66.7\)
a,PTHH:2Al+6HCl->2AlCl3+3H2(1)
nAl=8,1/27=0,3(mol)
từ pthh(1)->\(\dfrac{3}{2}\)nAl=nH2=\(\dfrac{3}{2}\).0,3=0,45
->VH2=0,45.22,4=10,08(lít)
b,PTHH:3H2+Fe2O3->2Fe+3H2O(2)
từ pthh(2)->\(\dfrac{2}{3}\)nH2=nFe=0,45.\(\dfrac{2}{3}\)=0,3
->nFe=16,8(g)
mà thực tế chỉ thu được 11,2g nên hiệu suất phản ứng là \(\dfrac{11,2}{16,8}.100\approx66,6\%\)

\(PTHH:Fe+2HCl\rightarrow FeCl_2+H_2\)
________0,2____0,4______ 0,2_____0,2
a, Ta có:
\(n_{Fe}=\frac{11,2}{56}=0,2\left(mol\right)\)
\(\Rightarrow V_{H2}=0,2.22,4=4,48\left(l\right)\)
b,
\(m_{HCl}=0,4.\left(1+35,5\right)=14,6\left(g\right)\)
c,
\(m_{FeCl2}=0,2.\left(56+35,5.2\right)=25,4\left(g\right)\)
Fe+2HCl---------> FeCl2 + H2
\(n_{Fe}=\frac{11,2}{56}=0,2\left(mol\right)\)
a) Theo PT: \(n_{H_2}=n_{Fe}=0,2\left(mol\right)\)
=> V H2 = 0,2. 22,4 = 4,48(l)
b) Theo PT: \(n_{HCl}=2n_{Fe}=0,4\left(mol\right)\)
=> m HCl = 0,4. 36,5 = 14,6 (g)
c) Theo PT: \(n_{FeCl_2}=n_{Fe}=0,2\left(mol\right)\)
=> m FeCl2 = 0,2. 127 = 25,4 (g)

a) PTHH: Fe + 2HCl ===> FeCl2 + H2
nFe = 11,2 / 56 = 0,2 (mol)
=> nH2 = nFe = 0,2 mol
=> VH2(đktc) = 0,2 x 22,4 = 4,48 lít
nHCl = 2.nFe = 0,4 mol
=> mHCl = 0,4 x 36,5 = 14,6 gam
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(n_{Fe}=\frac{11,2}{56}=0,2\left(mol\right)\)
\(\Rightarrow n_{HCl}=2n_{Fe}=2.0,2=0,4\left(mol\right)\Rightarrow m_{HCl}=0,4.36,5=14,6\left(g\right)\)
\(n_{H2}=n_{Fe}=0,2\left(mol\right)\)
\(\Rightarrow V_{H2}=0,2.22,4=4,48\left(l\right)\)

nMg = \(\dfrac{6}{24}=0,25\left(mol\right)\)
Pt: Mg + 2HCl --> MgCl2 + H2
...0,25........0,5......................0,25
VH2 thu được = 0,25 . 22,4 = 5,6 (lít)
mHCl đã dùng = 0,5 . 36,5 = 18,25 (g)
c) nFe2O3 = \(\dfrac{16}{160}=0,1\left(mol\right)\)
Pt: Fe2O3 + 3H2 --to--> 2Fe + 3H2O
...................0,25 mol--> \(\dfrac{0,5}{3}\) mol
Xét tỉ lệ mol giữa Fe2O3 và H2:
\(\dfrac{0,1}{1}>\dfrac{0,25}{3}\)
Vậy Fe2O3 dư
mFe thu được sau pứ = \(\dfrac{0,5}{3}.56=9,33\left(g\right)\)

Số mol của Fe là :
nFe = 11,2/56 = 0,2 (mol)
Ta có PTHH :
Fe + 2HCl \(\rightarrow\) FeCl2 + H2\(\uparrow\)
1 mol 2 mol 1 mol 1 mol
0,2 mol 0,4 mol 0,2 mol 0,2 mol
a) Khối lượng FeCl2 tạo thành là :
mFeCl2 = 0,2.127 = 25,4 (g)
b) Thể tích H2 thu được ở đktc là :
VH2 = 0,2.22,4 = 4,48 (l)
c) Khối lượng của HCl là :
mHCl = 0,4.36,5 = 14,6 (g)
PTHH: Fe + 2HCl ===> FeCl2 + H2
a) nFe = 11,2 / 56 = 0,2 (mol)
Theo phương trình, nFeCl2 = nFe = 0,2 (mol)
=> Khối lượng FeCl2: mFeCl2 = 0,2 x 127 = 25,4 gam
b) Theo phương trình, nH2 = nFe = 0,2 (mol)
=> Thể tích H2 thu được: VH2(đktc) = 0,2 x 22,4 = 4,48 lít
c)
Cách 1: Áp dụng định luật bảo toàn khối lượng
=> mHCl = mFeCl2 + mH2 - mFe = 25,4 + 0,2 x 2 - 11,2 = 14,6 gam
Cách 2: Theo phương trình, nHCl = 2.nFe = 0,4 (mol)
=> mHCl = 0,4 x 36,5 = 14,6 gam

Câu 1:
a) - Điều chế O2:
.........2KClO3 --to--> 2KCl + 3O2
- Điều chế ZnO:
..........2Zn + O2 --to--> 2ZnO
- Điều chế H2, FeSO4:
..........Fe + H2SO4 (loãng) --> FeSO4 + H2
b) Pt: 2KClO3 --to--> 2KCl + 3O2
- Điều chế Al2O3:
..........4Al + 3O2 --to--> 2Al2O3
- Điều chế SO2:
...........S + O2 --to--> SO2
- Điều chế Fe3O4:
...........3Fe + 2O2 --to--> Fe3O4
c) - Điều chế H2:
............Zn + H2SO4 (loãng) --> ZnSO4 + H2
- Điều chế O2:
...........2KMnO4 --to--> K2MnO4 + MnO2 + O2
- Điều chế H2O:
...........2H2 + O2 --to--> 2H2O
- Điều chế H3PO4:
...........4P + 5O2 --to--> 2P2O5
...........P2O5 + 3H2O --> 2H3PO4
Câu 2:
nAlCl3 = \(\dfrac{26,7}{133,5}=0,2\) mol
Pt: 2Al + 6HCl --> 2AlCl3 + ....3H2
0,2 mol<----------- 0,2 mol-> 0,3 mol
mAl pứ = 0,2 . 27 = 5,4 (g)
VH2 = 0,3 . 22,4 = 6,72 (lít)
nH2O = \(\dfrac{9}{18}=0,5\) mol
Pt: .....2H2 + O2 --to--> 2H2O
...0,3 mol-------------> 0,3 mol
...CH4 + 2O2 --to--> CO2 + 2H2O
0,1 mol<--------------------(0,5 - 0,3) mol
VCH4 cần dùng = 0,1 . 22,4 = 2,24 (lít)


Số mol
Phương trình
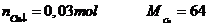
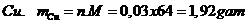
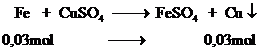
 khối lượng
khối lượng
Vậy khối lượng kim loại  là 1,92 gam
là 1,92 gam

PTHH: 2A + 6HCl -> 2ACl3 + 3H2
Ta có: \(n_{H_2}=\dfrac{5,04}{22,4}=0,225\left(mol\right)\)
Theo PTHH và đề bài, ta có:
\(n_A=\dfrac{2.0,225}{3}=0,15\left(mol\right)\)
=> \(M_A=\dfrac{4,08}{0,15}\approx27\left(\dfrac{g}{mol}\right)\)
Vậy: kim loại A (III) là nhôm (Al=27).
Ta có:
nH2 =5,04/22,4=0,225 (mol)
PTHH
2A+6HCl------> 2ACl3 +3H2
2 6 6 3
0.15 <------------------------0,225 (mol)
MA= 4,08/0,15=27-> Nhôm
=> A là Nhôm(Al)
a. \(n_{Fe}=\frac{m}{M}=\frac{5,6}{56}=0,1mol\)
PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
Ban đầu: 0,1 0,1 mol
Trong pứng: 0,05 0,1 0,05 mol
Sau pứng: 0,05 0 0,05 mol
\(\rightarrow n_{H_2}=n_{Fe}=0,1mol\)
\(\rightarrow V_{H_2\left(ĐKTC\right)}=n.22,4=0,1.22,4=2,24l\)
b. \(n_{Fe}=\frac{m}{M}=\frac{5,6}{56}=0,1mol\)
\(\rightarrow n_{H_2}=n_{HCl}=\frac{0,1.1}{2}=0,05mol\)
\(\rightarrow V_{H_2}=n.22,4=0,05.22,4=1,12l\)