Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Công thức về khối lượng phản ứng:
mCaCO3 = mCaO + mCO2
b) Áp dụng định luật bảo toàn khối lượng ta có :
mCaCO3 = 140 + 110 = 250 kg
Tỉ lệ phần trăm của Canxi cacbonat có trong đá vôi là :
%mCaCO3 = \(\frac{250.100\text{%}}{280}\) = 89,28%.

a) mCaCO3 = mCaO + mCO2
b) Khối lượng của CaCO3 đã phản ứng:
140 + 110 = 250 kg
Tỉ lệ phần trăm khối lượng CaCO3 chứa trong đá vôi:
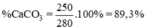

a) Công thức về khối lượng phản ứng:
mCaCO3 = mCaO + mCO2
b) mCaCO3 = 280 + 110 = 390 kg
=> %CaCO3
= \(\frac{390}{560}\) = 69,7%

a.
không vì sau phản ứng đã có lượng khí cacbonic thoát ra.
b.
theo định luật bảo toàn khối lượng, ta có công thức về khối lượng: m đá vôi + m HCl = m CaCl 2 + m CO 2 15 + 25 = 33,4 + m CO 2 m CO 2 = (15 + 25) - 33,4 = 40 - 33,4 = 6,6 (g)

a) PTHH: CaO + H2O ===> Ca(OH)2
b) nCaO = 2,8 / 56 = 0,05 (mol)
=> nCa(OH)2 = nCaO = 0,05 (mol)
=> mCa(OH)2 = 0,05 x 74 = 3,7 (gam)
a) Ta có:
nCaO= \(\frac{m_{CaO}}{M_{CaO}}=\frac{2,8}{56}=0,05\left(mol\right)\)
PTHH: CaO + H2O -> Ca(OH)2
b) Theo PTHH và đề bài, ta có:
\(n_{Ca\left(OH\right)_2}=n_{CaO}=0,05\left(mol\right)\)
Khối lượng Ca(OH)2 thu được:
\(m_{Ca\left(OH\right)_2}=n_{Ca\left(OH\right)_2}.M_{Ca\left(OH\right)_2}=0,05.74=3,7\left(g\right)\)

CaC2 + 2H2O -> Ca(OH)2 + C2H2
Theo ĐLBTKL cho PTHH trên ta có:
mCaC2+ mH2O=mCa(OH)2+mC2H2
=>mCaC2=74+26-36=64(kg)
%mCaC2=\(\dfrac{64}{80}.100\%=80\%\)

\(a.Ca+H_2O\rightarrow Ca\left(OH\right)_2+H_2\\ CaO+H_2O\rightarrow Ca\left(OH\right)_2\\ b.n_{H_2}=n_{Ca}=0,1\left(mol\right)\\ \Rightarrow m_{Ca}=0,1.40=4\left(g\right)\\ \Rightarrow m_{CaO}=9,6-4=5,6\left(g\right)\\ c.n_{CaO}=\dfrac{5,6}{56}=0,1\left(mol\right)\\ \Sigma n_{Ca\left(OH\right)_2}=n_{Ca}+n_{CaO}=0,1+0,1=0,2\left(mol\right)\\ \Rightarrow m_{Ca\left(OH\right)_2}=0,2.74=14,8\left(g\right)\)
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ pthh:Ca+2H_2O\rightarrow Ca\left(OH\right)_2+H_2\)
0,1 0,1 0,1
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)(2)
\(m_{Ca}=0,1.40=4\left(g\right)\\
m_{CaO}=9,6-4=5,6\left(g\right)\)
\(n_{CaO}=\dfrac{5,6}{56}=0,1\left(mol\right)\\
n_{Ca\left(OH\right)_2\left(2\right)}=n_{CaO}=0,1\left(mol\right)\)
\(n_{Ca\left(OH\right)_2}=\left(0,1+0,1\right).74=14,8\left(g\right)\)

mdd = 2,8 + 400 = 402,8 (g)
( m = D.V. TLR của nước là 1g/ml => 400g )
Áp dụng ĐLBTKL
a, CaO + H2O--> Ca(OH)2
b, tỉ lệ : 1:1
c, mCaO:mH2O=56:18=28:9
d, 200ml nước= 200g
=> mdd Ca(OH)2= mCaO + mH2O= 5,6 + 200=205 , 6g
Ta có n Ca(OH)2=nCaO=5,6/56=0,1 mol= nCa(OH)2
=> mCa(OH)2=0,1.74=7,4 g