Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

ta có pthh :C2H5OH +3O2 ---------->2CO2 +3H2O
Tỳ lệ :0,2 mol-----0,6 mol-----0,4 mol (hiểu tại sao hông )
VCO2 :0,4 X 22,4 =(MÁY TÍNH ?)
nCO2=0,6mol -------->n KK =0,6 X 100/20 =3 MOL
Vkk =3 x 22,4 =67,2 l

a.

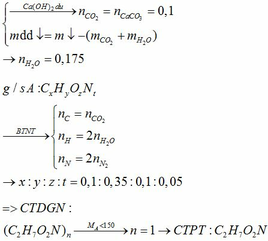
b.
Vì A pứ với NaOH nên CTCT của A là: CH3COONH4 hoặc HCOONH3CH3
Y pứ ở 15000C nên Y là: CH4
=> X: CH3COONa → A:CH3COONH4
Z: CH≡CH → T: CH3CHO
Vậy A là: CH3COONH4 (amoniaxetat)

a) MX = 146g/mol
VCO2 : VH2O = 6 : 5
=> nC : nH = 3 : 5
=> CTĐGN: (C3H5Oa)n
→ (41 + 16a).n = 146 → (a; n) = (4; 2) → X: C6H10O4
b) C6H10O4 + 6,5O2 → 6CO2 + 5H2O
0,05 0,325
=> p = 7,3g
c)
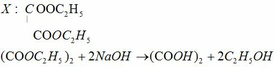


Do lấy dư 20% oxi so với lượng cần đốt cháy nên lượng oxi đã lấy là:


Tổng khối lượng CO2 và SO2 :
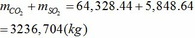
Chú ý:
Lượng O2 lấy dư 20% so với với lượng cần thiết => tính mol O2 chính xác

A tác dụng với NaHCO3 cho khí CO2 → A: axit CH3COOH
BTKL: m + mO2 = mCO2 + mH2O => m = 1,8
=> nCH3COOH = 0,03
CH3COOH + C2H5OH → CH3COOC2H5 + H2O
0,03 0,02 0,0125
=> H = 62,5%
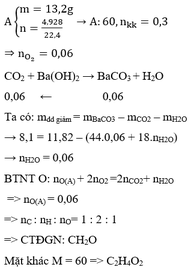
a) 2CxHy + \(\dfrac{4x+y}{2}\)O2 --to--> 2xCO2 + yH2O
b) \(n_A=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{CO_2}=\dfrac{26,4}{44}=0,6\left(mol\right)\)
=> nC = 0,6 (mol)
Số nguyên tử C = \(\dfrac{0,6}{0,3}=2\) (nguyên tử)
\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\)
=> nH = 0,6 (mol)
Số nguyên tử H = \(\dfrac{0,6}{0,3}=2\) (nguyên tử)
=> CTPT: C2H2 (axetilen)
CTCT: \(CH\equiv CH\)
c)
PTHH: 2C2H2 + 5O2 --to--> 4CO2 + 2H2O
0,3--->0,75
=> VO2(lý thuyết) = 0,75.22,4 = 16,8 (l)
=> Vkk(lý thuyết) = 16,8.5 = 84 (l)
=> \(V_{kk\left(thực.tế\right)}=\dfrac{84.120}{100}=100,8\left(l\right)\)