Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

+) Trường hợp 1: Hỗn hợp gồm NaF và NaCl
PTHH: \(NaCl+AgNO_3\rightarrow AgCl\downarrow+NaNO_3\)
Ta có: \(n_{AgCl}=\dfrac{2,87}{143,5}=0,02\left(mol\right)=n_{NaCl}\)
\(\Rightarrow m_{NaCl}=0,02\cdot58,5=1,17\left(g\right)\) \(\Rightarrow m_{NaF}=0,415\left(g\right)\)
+) Trường hợp 2: Hỗn hợp không chứa NaF
Gọi công thức chung 2 muối là NaR
PTHH: \(NaR+AgNO_3\rightarrow NaNO_3+AgR\downarrow\)
Theo PTHH: \(n_{NaR}=n_{AgR}\) \(\Rightarrow\dfrac{1,595}{23+\overline{M}_R}=\dfrac{2,87}{108+\overline{M}_R}\)
\(\Rightarrow\overline{M}_R\approx83,3\) \(\Rightarrow\) 2 halogen cần tìm là Brom và Iot
Vậy 2 muối có thể là (NaF và NaCl) hoặc (NaBr và NaI)
*P/s: Các phần còn lại bạn tự làm

a,
- Giả sử X là F (không tạo kết tủa) \(\Rightarrow\) Y là Cl.
\(AgNO_3+NaCl\rightarrow NaCl+AgNO_3\)
\(\rightarrow n_{NaCl}=n_{AgCl}=0,331\left(mol\right)\)
\(\Rightarrow m_{NaCl}=19,36< 22\left(g\right)\left(TM\right)\)
- Giả sử X, Y đều tạo kết tủa. Gọi chung là R.
nNaR= nAgR
\(\Rightarrow\frac{22}{23+R}=\frac{47,5}{108+R}\)
\(\Leftrightarrow47,5\left(23+R\right)=22\left(108+R\right)\)
\(\Leftrightarrow R=50,3\left(Cl;Br\right)\left(TM\right)\)
Vậy NaX, NaY có thể là NaF, NaCl hoặc NaCl, NaBr.
b,
- Trường hợp NaF, NaCl:
mNaCl= 19,36g
\(\Rightarrow C\%_{NaCl}=\frac{19,36.100}{200}=9,68\%\)
\(m_{NaF}=22-19,36=2,64\left(g\right)\)
\(\Rightarrow C\%_{NaF}=\frac{2,64.100}{200}=1,32\%\)
Trường hợp NaCl, NaBr
Gọi x là mol NaCl; y là mol NaBr
Bảo toàn nguyên tố, n muối= n kết tủa
\(\Rightarrow58,5x+103y=22;143,5x+188y=47,5\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)
\(C\%_{NaCl}=\frac{0,2.58,5.100}{200}=5,85\%\)
\(C\%_{NaBr}=\frac{0,1.103.100}{200}=5,15\%\)

Chọn A
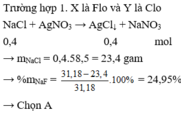
Chú ý: Với đề trắc nghiệm chọn được đáp án A có thể không cần xét thêm trường hợp 2.
Trường hợp 2. X khác Flo. Gọi hỗn hợp (NaX, NaY) tương đương với NaM


Kết tủa `AgCl`: \(\dfrac{4,305}{143,5}=0,03\left(mol\right)\)
Có: \(\left(\overline{M}+35,5\right).0,03=1,915\left(g\right)\Rightarrow\overline{M}=28,33\)
=> \(\left\{{}\begin{matrix}A:Na\\B:K\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}x+y=0,1\\58,5x+74,5y=1,915\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,02\\y=0,01\end{matrix}\right.\)
\(\Rightarrow X:\left\{{}\begin{matrix}m_{NaCl}=1,17\left(g\right)\\m_{KCl}=0,745\left(g\right)\end{matrix}\right.\)

Giả xử Mx<My
Th1 cho x là flo y là cl
NACL+AgNO3=Agcl+nano3
0.4 0.4
mnacl=23.4 <mhh=31.84
==>TH1 thoả mãn mnaf=8.44
TH2 gọi CTchung của x.y là z
NAF +AgNO3=>AgZ+NANO3
31.84/23+Mz 57.34/108+Mz
-->Mz=83.13 -->X :Br Y:I
sau đó bn viết rõ pthh ra lập hệ pt là tính dc m các chất

1.
Gọi CT chung của 2 kim loại là M
M + 2HCl --> MCl2 + H2 (1)
MCl2 +2AgNO3 --> M(NO3)2 + 2AgCl (2)
nM=\(\dfrac{8,8}{M_M}\)(mol)
theo (1) : nAgNO3=2nM=\(\dfrac{17,6}{M_M}\left(mol\right)\)
Khi thêm 0,5 mol AgNO3 thì không kết tủa hết , còn khi thêm 0,7 mol AgNO3 vào dd D thì AgNO3 dư
=> 0,5 < \(\dfrac{17,6}{M_M}\)< 0,7 => 25,14 < MM<35,2
=> 2 kim loại lần lượt là Na và K
2.
a) Gọi CT chung của 2 muối natri của 2 halogen là NaX
NaX + AgNO3 --> NaNO3 + AgX (1)
nNaX=\(\dfrac{22}{23+M_X}\)(mol)
nAgX=\(\dfrac{47,5}{108+M_X}\)(mol)
Theo (1) :nNaX=nAgX => \(\dfrac{22}{23+M_X}=\dfrac{47,5}{108+M_X}\)
=> MX=50,33(g/mol)
=> 2 halogen là : Cl2 và Br2
b) Gía sử có x mol NaCl
y mol NaBr
=> \(\left\{{}\begin{matrix}58,5x+103y=22\\143,5x+188y=47,5\end{matrix}\right.=>\left\{{}\begin{matrix}x=0,2\left(mol\right)\\y=0,1\left(mol\right)\end{matrix}\right.\)
=> mNaCl=11,7(g)
mNaBr=10,3(g)

- Nếu một trong 2 muối là NaF => Muối còn lại là NaCl
\(n_{AgCl}=\dfrac{68,306}{143,5}=0,476\left(mol\right)\)
PTHH: NaCl + AgNO3 --> NaNO3 + AgCl
0,476<-----------------------0,476
=> mNaCl = 0,476.58,5 = 27,846(g)
=> mNaF = 35,411 - 27,846 = 7,565(g)
- Nếu trong A không có NaF
=> Gọi công thức của 2 muối là NaX
=> \(n_{NaX}=\dfrac{35,411}{23+M_X}\left(mol\right)\)
PTHH: NaX + AgNO3 --> NaNO3 + AgX
\(\dfrac{35,411}{23+M_X}\)----------------->\(\dfrac{35,411}{23+M_X}\)
=> \(\dfrac{35,411}{23+M_X}=\dfrac{68,306}{108+M_X}\)
=> \(M_X=68,5\)
=> 2 muối là NaCl, NaBr
Gọi số mol của NaCl, NaBr là a, b
=> 58,5a + 103b = 35,411
PTHH: NaCl + AgNO3 --> AgCl + NaNO3
a------------------>a
NaBr + AgNO3 --> AgBr + NaNO3
b------------------->b
=> 143,5a + 188b = 68,306
=> a = 0,1; b = 0,287
=> \(\left\{{}\begin{matrix}m_{NaCl}=0,1.58,5=5,85\left(g\right)\\m_{NaBr}=0,287.103=29,561\left(g\right)\end{matrix}\right.\)