Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) \(2KNO_3\underrightarrow{t^o}2KNO_2+O_2\)
Phản ứng phân hủy
b) \(n_{O_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\)
PTHH: 2KNO3 --to--> 2KNO2 + O2
0,15<--------------------0,075
=> \(m_{KNO_3\left(PTHH\right)}=0,15.101=15,15\left(g\right)\)
=> mKNO3 (thực tế) = \(\dfrac{15,15.100}{85}=17,824\left(g\right)\)
c) \(n_{KNO_3\left(pư\right)}=\dfrac{10,1.80\%}{101}=0,08\left(mol\right)\)
=> nO2 = 0,04 (mol)
=> VO2 = 0,04.22,4 = 0,896(l)

a) PTHH:
2KNO3→2KNO2 + O2
b)\(n_{O_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\)Theo PTHH ta có:
nKNO3=2nO2=0,15(mol)
mKNO3 ban đầu=0,15.101=15,15(g)
mKNO3 thực tế=15,15.\(\dfrac{85}{100}\)=12,8775(g)

nK=0,2(mol)
PTHH: 4K + O2 -to-> 2 K2O
nK2O= 0,1(mol) => mK2O=0,1.94=9,4(g)
nO2=0,05(mol) -> V(O2,đktc)=0,05.22,4=1,12(l)
V(kk,dktc)=5.V(O2,dktc)=5.1,12=5,6(l)

a, \(2Zn+O_2\underrightarrow{t^o}2ZnO\)
b, \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
Theo PT: \(n_{O_2}=\dfrac{1}{2}n_{Zn}=0,1\left(mol\right)\Rightarrow V_{O_2}=0,1.22,4=2,24\left(l\right)\)
\(\Rightarrow V_{kk}=5V_{O_2}=11,2\left(l\right)\)
c, \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
Theo PT: \(n_{KMnO_4}=2n_{O_2}=0,2\left(mol\right)\Rightarrow m_{KMnO_4}=0,2.158=31,6\left(g\right)\)

nMg = 7,2/24 = 0,3 (mol)
PTHH: 2Mg + O2 -> (t°) 2MgO
Mol: 0,3 ---> 0,15 ---> 0,3
VO2 = 0,15 . 22,4 = 3,36 (l)
Vkk = 3,36 . 5 = 16,8 (l)
mMgO = 0,3 . 40 = 12 (g)

a)PTHH:2KClO\(_3\)➞\(^{t^o}\)2KCl+3O\(_2\)
b) n\(_{KClO_3}\)=\(\dfrac{m_{KClO_3}}{M_{KClO_3}}\)=\(\dfrac{12,15}{122,5}\)\(\approx\)0,1(m)
PTHH : 2KClO\(_3\) ➞\(^{t^o}\) 2KCl + 3O\(_2\)
tỉ lệ : 2 2 3
số mol : 0,1 0,1 0,15
V\(_{O_2}\)=n\(_{O_2}\).22,4=0,15.22,4=3,36(l)
c)PTHH : 2Zn + O\(_2\) -> 2ZnO
tỉ lệ : 2 1 2
số mol :0,3 0,15 0,3
m\(_{Zn}\)=n\(_{Zn}\).M\(_{Zn}\)=0,3.65=19,5(g)

4P+5O2-to>2P2O5
0,04----0,05----0,02
n P=0,04 mol
=>m P2O5=0,02.142=2,84g
=>VO2=0,05.22,4=1,12l
c)
2KMnO4-to>K2MnO4+MnO2+O2
0,1----------------------------------------0,05
H=10%
m KMnO4=0,1.158.110%=17,28g
\(n_P=\dfrac{1,24}{31}=0,04\left(mol\right)\\ pthh:4P+5O_2\underrightarrow{T^O}2P_2O_5\)
0,04 0,05 0,02
=> \(\left\{{}\begin{matrix}m_{P_2O_5}=0,02.142=2,84\left(g\right)\\V_{O_2}=0,05.22,4=1,12\left(l\right)\end{matrix}\right.\)
\(pthh:2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
0,1 0,05
=> \(m_{KMnO_4}=0,1.158=15,8\left(g\right)\)
\(m_{KMnO_4\left(d\text{ùng}\right)}=15,8.110\%=17,38\left(g\right)\)

Bài 1
2KClO3--->2KCl+3O2
Theo pthh
n O2=3/2n KClO3=0,75(mol)
m O2=0,75.32=24(g)
Bài 2
a)2KNO3-->2KNO2+O2
b)n O2=1,68/22,4=0,075(mol)
Theo pthh
n KNO3=2n O2=0,15(mol)
m KNO3=0,15.101=15,15(g)
H=85%
-->m KNO3=12,8775(g)
Bài 3
2KClO3--->2KCl+3O2
2O2+CH4--->CO2+2H2O
O2+2H2--->2H2O
Theo pthh2
n O2=2n CH4=1(mol)
Theo pthh3
n O2=1/2n H2=0,125(mol)
\(\sum n_{O2}\) cần =0,125+1=1,125(mol)
Theo pthh1
n KClO3=2/3 n O2=0,75(mol)
m KClO3=0,75.122,5=91,875(g)
Bài 3
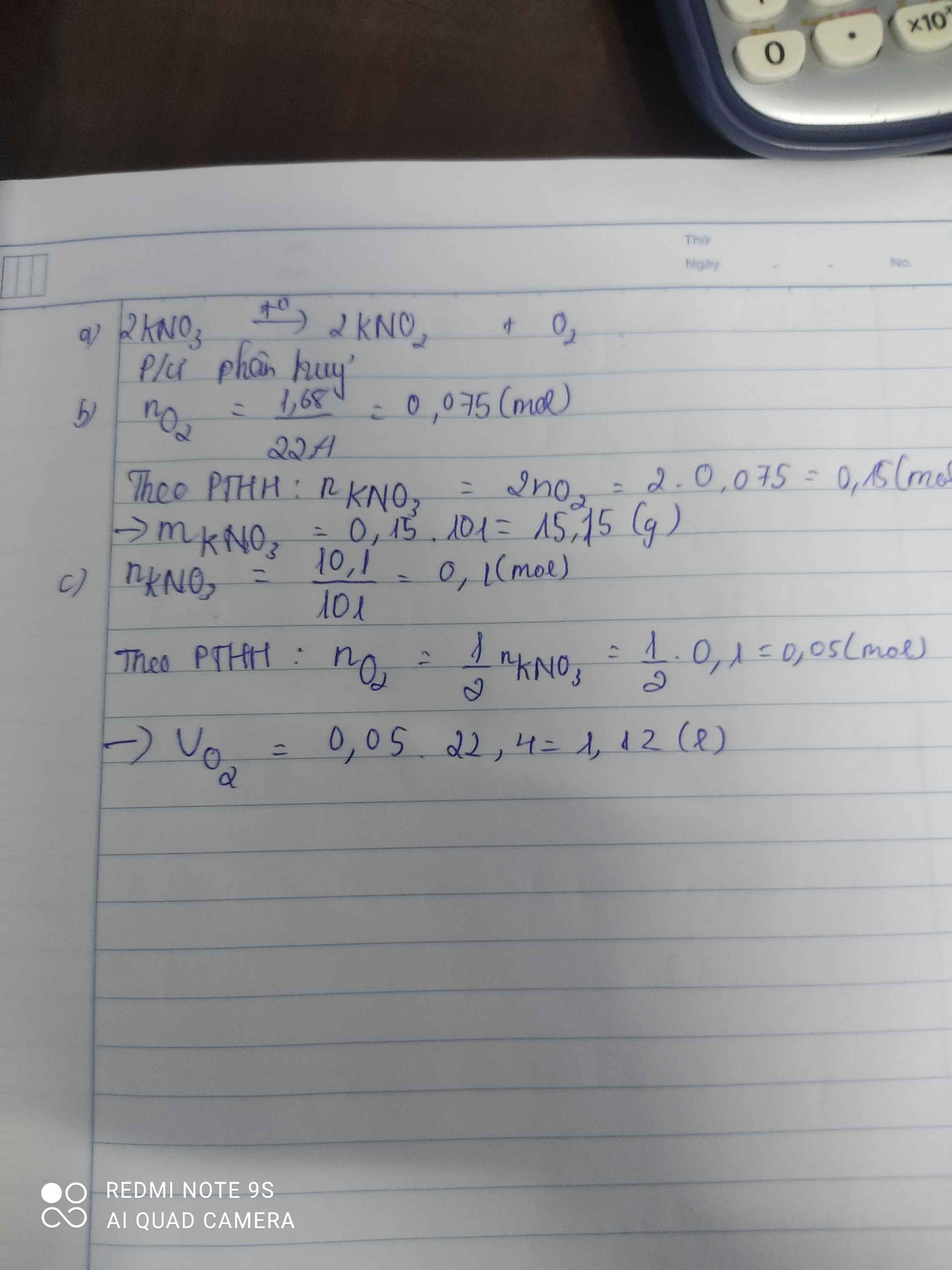

Bài 1.
\(n_{Mg}=\dfrac{2,4}{24}=0,1mol\)
\(2Mg+O_2\underrightarrow{t^o}2MgO\)
Đây là phản ứng hóa hợp vì chất sản phẩm được tạo từ 2 chất ban đầu.
\(n_{O_2}=2n_{Mg}=0,2mol\)
\(V=0,2\cdot22,4=4,48\left(l\right)\)
Bài 2.
\(2KNO_3\underrightarrow{t^o}2KNO_2+O_2\)
\(n_{O_2}=\dfrac{1,68}{22,4}=0,075mol\)
\(n_{KNO_3}=2n_{O_2}=0,15mol\)\(\Rightarrow m_{KNO_3}=0,15\cdot101=15,15g\)