Cho 12g hỗn hợp Cao và Feo tác dụng với 100ml dd H2SO4 2M. Tính % khối lượng từng chất trong hỗn hợp
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) Gọi `n_{CuO} = a (mol); n_{ZnO} = b (mol)`
`=> 80a + 81b = 12,1(1)`
`n_{HCl} = 3.0,1 = 0,3 (mol)`
PTHH:
`CuO + 2HCl -> CuCl_2 + H_2O`
`ZnO + 2HCl -> ZnCl_2 + H_2O`
Theo PT: `n_{HCl} = 2n_{ZnO} + 2n_{CuO}`
`=> 2a + 2b = 0,3 (2)`
Từ `(1), (2) => a = 0,05; b = 0,1`
`=> \%m_{CuO} = (0,05.80)/(12,1) .100\% = 33,06\%`
`=> \%m_{ZnO} = 100\% - 33,06\% = 66,94\%`
b) PTHH:
`CuO + H_2SO_4 -> CuSO_4 + H_2O`
`ZnO + H_2SO_4 -> ZnSO_4 + H_2O`
Theo PT: `n_{H_2SO_4} = n_{CuO} + n_{ZnO} = 0,15 (mol)`
`=> m_{ddH_2SO_4} = (0,15.98)/(20\%) = 73,5 (g)`

\(n_{H_2}=\dfrac{2,24}{22,4}=0,1mol\)
a)\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,1 0,1 0,1
\(m_{Fe}=0,1\cdot56=5,6\left(g\right)\)
b)\(\Rightarrow\%m_{Fe}=\dfrac{5,6}{12}\cdot100\%=46,67\%\) \(\Rightarrow\%m_{Cu}=100\%-46,67\%=53,33\%\)
c)\(n_{NaOH}=0,1\cdot1=0,1mol\)
\(2NaOH+FeCl_2\rightarrow Fe\left(OH\right)_2+2NaCl\)
0,1 0,1 0,1
\(m_{Fe\left(OH\right)_2}=0,1\cdot90=9\left(g\right)\)

\(n_{H_2}=\dfrac{3,36}{22,4}=0,15mol\\ a)ZnO+H_2SO_4\rightarrow ZnSO_4+H_2O\\ Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,15 0,15 0,15 0,15
\(b)m_{Fe}=0,15.56=8,4g\\ m_{ZnO}=16,5-8,4=8,1g\\ c)n_{ZnO}=\dfrac{8,1}{81}=0,1mol\\ ZnO+H_2SO_4\rightarrow ZnSO_4+H_2O\)
0,1 0,1 0,1 0,1
\(V_{ddH_2SO_4}=\dfrac{0,15+0,1}{2}=0,125M\\ d)Fe+CuSO_4\rightarrow FeSO_4+Cu\)
0,15 0,15 0,15 0,15
\(m_{rắn}=m_{ZnO}+m_{Cu}=8,1+0,15.64=17,7g\)

vì đề không nói là H2SO4 đặc nóng nên mình coi là đặc nguội nha. H2SO4 đặc nguội thụ động với Fe nên không xảy ra phản ứng.

a) \(2Al+6HCl\rightarrow2AlCl_3+3H_2\left(1\right)\\ Fe+2HCl\rightarrow FeCl_2+H_2\left(2\right)\\ 2Al+2NaOH+2H_2O\rightarrow2NaAlO_2+3H_2\)
Cho hỗn hợp tác dụng với NaOH, chất rắn không tan là Fe
=> mFe= 1,12 (g) \(\Rightarrow n_{Fe}=0,02\left(mol\right)\)
Ta có: \(n_{H_2\left(2\right)}=n_{Fe}=0,02\left(mol\right)\)
=> \(n_{H_2\left(1\right)}=\Sigma n_{H_2}-n_{H_2\left(2\right)}=0,065-0,02=0,045\left(mol\right)\)
\(\Rightarrow n_{Al}=\dfrac{2}{3}n_{H_2\left(1\right)}=0,03\left(mol\right)\)
\(\Rightarrow m_{Al}=0,03.27=0,81\left(g\right)\)
\(\Rightarrow\%m_{Al}=41,97\%,\%m_{Fe}=58,03\%\)
b) \(m_{FeCl_2}=0,02.127=2,54\left(g\right)\\ m_{AlCl_3}=0,03.133,5=4,005\left(g\right)\)
Cho 24g hỗn hợp CuO và Fe2O3 tác dụng với 800ml dd HCL 1M. Tính % khối lượng từng chất trong hỗn hợp

Gọi `n_{CuO} = a (mol); n_{Fe_2O_3} = b (mol)`
`=> 80x + 160y = 24 (1)`
PTHH:
`CuO + 2HCl -> CuCl_2 + H_2O`
`Fe_2O_3 + 6HCl -> 2FeCl_3 + 3H_2O`
Theo PT: `n_{HCl} = 2n_{CuO} + 6n_{Fe_2O_3}`
`=> 2x + 6y = 0,8.1 = 0,8 (2)`
Từ `(1), (2) => x = y = 0,1`
`=>` \(\left\{{}\begin{matrix}\%m_{CuO}=\dfrac{0,1.80}{24}.100\%=33,33\%\\\%m_{Fe_2O_3}=100\%-33,33\%=66,67\%\end{matrix}\right.\)

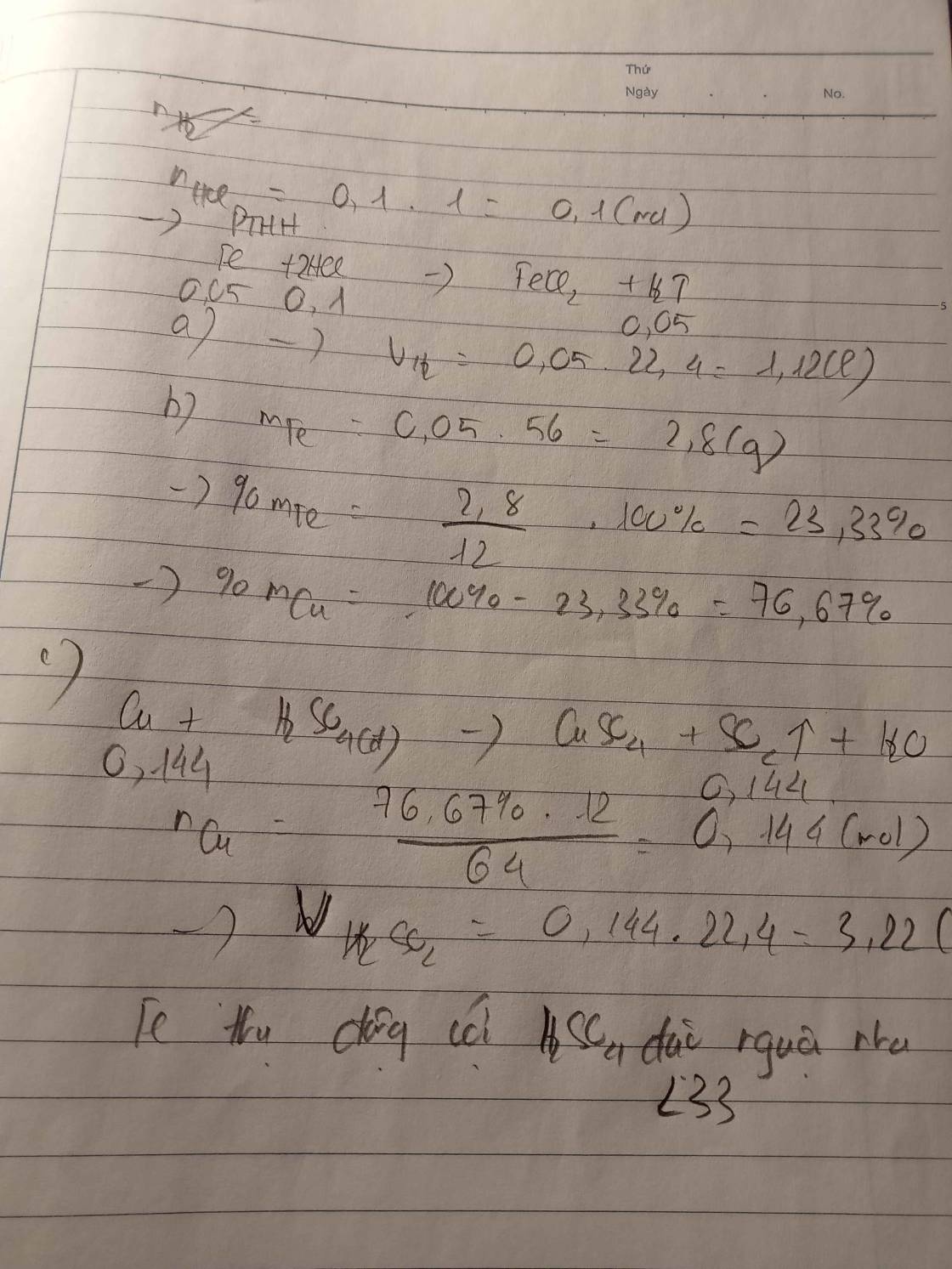

Gọi $n_{CaO} = a(mol) ; n_{FeO} =b (mol)$
$\Rightarrow 56a + 72b = 12(1)$
$CaO + H_2SO_4 \to CaSO_4 + H_2O$
$FeO + H_2SO_4 \to FeSO_4 + H_2O$
Theo PTHH : $n_{H_2SO_4} = a + b = 0,1.2 = 0,2(2)$
Từ (1)(2) suy ra : a = 0,15 ; b = 0,05
$\%m_{CaO} = \dfrac{0,15.56}{12}.100\% = 70\%$
$\%m_{FeO} = 100\% - 70\% = 30\%$