Trộn 200ml dung dịch NaC1 0,1M với 300ml dung dịch Na2CO3 0,1M. Tính nồng độ các ion trong dung dịch thu được? Cần gấppp ạa
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a, \(n_{HCl}=0,2.0,1=0,02\left(mol\right)=n_{H^+}=n_{Cl^-}\)
\(n_{H_2SO_4}=0,2.0,15=0,03\left(mol\right)=n_{SO_4^{2-}}\) \(\Rightarrow n_{H^+}=2n_{H_2SO_4}=0,06\left(mol\right)\)
\(\Rightarrow\Sigma n_{H^+}=0,02+0,06=0,08\left(mol\right)\)
\(n_{Ba\left(OH\right)_2}=0,3.0,05=0,015\left(mol\right)=n_{Ba^{2+}}\)
\(\Rightarrow n_{OH^-}=2n_{Ba\left(OH\right)_2}=0,03\left(mol\right)\)
\(H^++OH^-\rightarrow H_2O\)
0,03___0,03 (mol) ⇒ nH+ dư = 0,05 (mol)
\(Ba^{2+}+SO_4^{2-}\rightarrow BaSO_4\)
0,015___0,015______0,015 (mol) ⇒ nSO42- dư = 0,015 (mol)
⇒ m = mBaSO4 = 0,015.233 = 3,495 (g)
\(\left[Cl^-\right]=\dfrac{0,02}{0,2+0,3}=0,04\left(M\right)\)
\(\left[H^+\right]=\dfrac{0,05}{0,2+0,3}=0,1\left(M\right)\)
\(\left[SO_4^{2-}\right]=\dfrac{0,015}{0,2+0,3}=0,03\left(M\right)\)
b, pH = -log[H+] = 1
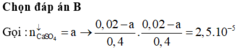

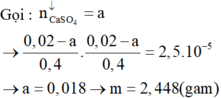
\(n_{NaCl}=0,1.0,2=0,02\left(mol\right)\)
\(m_{Na_2CO_3}=0,1.0,3=0,03\left(mol\right)\)
\(\left\{{}\begin{matrix}n_{Na^+}=0,02+0,03.2=0,08\left(mol\right)\\n_{Cl^-}=0,02\left(mol\right)\\n_{CO_3^{2-}}=0,03\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}C_{M\left(Na^+\right)}=\dfrac{0,08}{0,2+0,3}=0,16M\\C_{M\left(Cl^-\right)}=\dfrac{0,02}{0,2+0,3}=0,04M\\C_{M\left(CO_3^{2-}\right)}=\dfrac{0,03}{0,2+0,3}=0,06M\end{matrix}\right.\)