trộn 200g dung dịch Na2CO3 13,25% vào 300g dung dịch BaCl2 20,8%
Tính nồng độ % của dung dịch sau khi phản ứng. Biết :
Na2CO3 + BaCl2 -> 2NaCl + BaCl
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có :
nNa2CO3=200.13,25%\106=0,25(mol)
nBaCl2=350.20,8%\208=0,35(mol)
Na2CO3+BaCl2→BaCO3+2NaCl
Ta thấy : nNa2CO3=0,25<nBaCl2=0,35
nên BaCl2dư
Theo phương trình , có :
nBaCl2(pư)=nBaCO3=nNa2CO3=0,25(mol)
nNaCl=2nNa2CO3=0,25.2=0,5(mol)
⇒nBaCl2(dư)=0,35−0,25=0,1(mol)
Sau phản ứng,
mdd=ndd Na2CO3+mdd BaCl2−mBaCO3
=200+350−0,25.197=500,75(gam)
Vậy :
C%BaCl2(dư)=0,1.208\500,75.100%=4,15%
C%NaCl=0,5.58,5\500,75.100%=5,84%
%tk

. Do trộn 100g với 100g mà lượng dung dịch thu được < 200g thì muối sunfat kim loại là muối axit.( do sự thất thoát khí )
pt : 2MHSO4 + 2NaHCO3 = M2SO4 + Na2SO4 + 2CO2 + 2H2O
Sự thoát khí CO2 làm giảm khối lượng ( số mol CO2 = số mol NaHCO3 0,05mol)
gọi số mol của MHSO4 là x ta có:
(M + 97) x = 13,2 => x = 13,2/ (M + 97)
Theo phương trình sự tạo kết tủa với BaCl2 là muối sunfat:
MNaSO4 + BaCl2 = BaSO4 + MCl + NaCl
=> Với 0,1 < x < 0,1 + 0,02 thì 13< M < 35 thoả mãn Na = 23 Vậy công thức sunfat là NaHSO4

a) Vì: mA < 400 (g) nên phải có khí thoát ra → muối có dạng MHSO4 và khí là: CO2
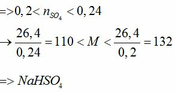
b)
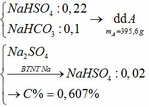
c) Tác dụng được với: MgCO3, Ba(HSO3)2, Al2O3, Fe(OH)2, Fe, Fe(NO3)2
Pt: 2NaHSO4 + MgCO3 → Na2SO4 + MgSO4 + CO2↑ + H2O
2NaHSO4 + Ba(HSO3)2 → BaSO4 + Na2SO4 + SO2↑ + 2H2O
6NaHSO4 + Al2O3 → 3Na2SO4 + Al2(SO4)3 + 3H2O
2NaHSO4 + Fe(OH)2 → Na2SO4 + FeSO4 + 2H2O
2NaHSO4 + Fe → Na2SO4 + FeSO4 + H2↑
12NaHSO4 + 9Fe(NO3)2 → 5Fe(NO3)3 + 2Fe2(SO4)3 + 6Na2SO4 + 3NO↑ + 6H2O

Ta có: \(n_{Na_2CO_3}=0,4.1=0,4\left(mol\right)\)
PT: \(Na_2CO_3+2HCl\rightarrow2NaCl+CO_2+H_2O\)
a, \(n_{HCl}=2n_{Na_2CO_3}=0,8\left(mol\right)\)
\(\Rightarrow C_{M_{HCl}}=\dfrac{0,8}{0,6}=\dfrac{4}{3}\left(M\right)\)
b, \(n_{NaCl}=2n_{Na_2CO_3}=0,8\left(mol\right)\Rightarrow m_{NaCl}=0,8.58,5=46,8\left(g\right)\)
\(n_{CO_2}=n_{Na_2CO_3}=0,4\left(mol\right)\Rightarrow V_{CO_2}=0,4.24,79=9,916\left(l\right)\)
c, \(C_{M_{NaCl}}=\dfrac{0,8}{0,4+0,6}=0,8\left(M\right)\)

\(\begin{cases} m_{H_2SO_4}=\dfrac{100.19,6\%}{100\%}=19,6(g)\\ m_{BaCl_2}=\dfrac{300.20,8\%}{100\%}=62,4(g) \end{cases} \Rightarrow \begin{cases} n_{H_2SO_4}=\dfrac{19,6}{98}=0,2(mol)\\ n_{BaCl_2}=\dfrac{62,4}{208}=0,3(mol) \end{cases}\\ a,PTHH:BaCl_2+H_2SO_4\to BaSO_4\downarrow +2HCl\)
Vì \(\dfrac{n_{H_2SO_4}}{1}<\dfrac{n_{BaCl_2}}{1}\) nên \(BaCl_2\) dư
\(\Rightarrow n_{BaSO_4}=0,2(mol)\\ \Rightarrow m_{BaSO_4}=0,2.233=46,6(g)\)
\(b,n_{HCl}=n_{BaSO_4}=0,2(mol)\\ \Rightarrow m_{CT_{HCl}}=0,2.36,5=7,3(g)\\ m_{dd_{HCl}}=100+300-46,6=353,4(g)\\ \Rightarrow C\%_{HCl}=\dfrac{7,3}{353,4}.100\%\approx 2,07\%\)
\(n_{Na_2CO_3}=\dfrac{200.13,25%}{100\%.106}=0,25(mol)\\ n_{BaCl_2}=\dfrac{20,8\%.300}{100\%.208}=0,3(mol)\\ PTHH:Na_2CO_3+BaCl_2\to BaSO_4\downarrow +2NaCl\)
Vì \(\dfrac{n_{Na_2CO_3}}{1}<\dfrac{n_{BaCl_2}}{1}\) nên \(BaCl_2\) dư
Do đó dd sau p/ứ gồm \(BaCl_2\) dư và \(NaCl\)
\(n_{BaSO_4}=0,25(mol);n_{NaCl}=0,5(mol);n_{BaCl_2(dư)}=0,3-0,25=0,05(mol)\\ \Rightarrow m_{NaCl}=0,5.58,5=29,25(g);m_{BaCl_2(dư)}=0,05.208=10,4(g)\\ \Rightarrow C\%_{NaCl}=\dfrac{29,25}{200+300-0,25.233}.100\%=6,62\%\\ C\%_{BaCl_2(dư)}=\dfrac{10,4}{200+300-0,25.233}.100\%=2,35\%\)