Đốt cháy hoàn toàn 4,48 lít hỗn hợp C2H4 và C3H6 có tỉ khối hơi so với oxi là 1,09375, rồi cho toàn bộ sản phẩm vào 500ml dung dịch NaOH 1,8M thì thu được sản phẩm và nồng độ mol tương ứng là:
A. NaHCO3 0,2M và Na2CO3 0,8M
B. Na2CO3 0,6M và NaOH 0,1M dư
C. NaHCO3 0,02M và Na2CO3 0,8M
D. Chỉ thu được Na2CO3 0,4M



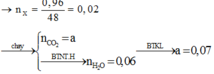
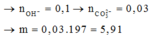
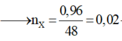
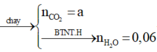
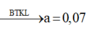
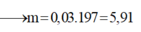





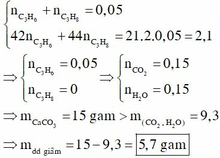
Đáp án A
Hướng dẫn
Dựa vào tỉ khối ta tính được khối lượng mỗi chất và số mol
n C O 2 = 0,2.2,5 = 0,5 (mol) và nNaOH = 0,9 mol
Tỉ lệ: T = n N a O H n C O 2 = 0 , 9 0 , 2 > 1 => Tạo 2 muối
NaOH + CO2 → NaHCO3
x x x
2NaOH + CO2 → Na2CO3 + H2O
2y y y
x + y = 0 , 5 x + 2 y = 0 , 9 ⇒ x = 0 , 1 y = 0 , 9
=> CNaHCO3 = 0 , 1 0 , 5 = 0,2 (M)
C N a H C O 3 = 0 , 4 0 , 5 0,8 (M)