cho 5,4 g hỗn hợp 2 kl ZN và Mg td vừa đủ với dd HCL thì được 6,72 l h2 ở đktc. tính khối lượng dd Hcl 14,6% đã dùng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(Zn+2HCl->ZnCl_2+H_2\\ Mg+2HCl->MgCl_2+H_2\\ n_{Zn}=a\\ n_{Mg}=b\\ 65a+24b=11,3g\\ n_{H_2}=a+b=\dfrac{6,72}{22,4}=0,3\\ a=0,1\\ m_{Zn}=65.0,1=6,5g\)

nH2= 0,3(mol)
PTHH: Mg +2HCl -> MgCl2 + H2
x_______2x______x_______x(mol)
Zn +2 HCl -> ZnCl2 + H2
y____2y____y______y(mol)
Ta có hpt: \(\left\{{}\begin{matrix}24x+65y=11,3\\x+y=0,3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)
=> m(muối)= mMgCl2+ mZnCl2= 95x+136y=95.0,2+136.0,1=32,6(g)

\(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\\
pthh:Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,2 0,1 0,1
\(m_{HCl}=0,2.36,5=7,3\left(g\right)\\
V_{H_2}=0,1.22,4=2,24l\\
m_{\text{dd}}=6,5+200-\left(0,1.2\right)=206,3g\)
bài 2 :
\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\\
pthh:Mg+2HCl\rightarrow MgCl_2+H_2\)
0,2 0,4 0,2 0,2
\(m_{HCl}=0,4.36,5=14,6g\\
V_{H_2}=0,2.22,4=4,48l\\
m\text{dd}=4,8+200-0,4=204,4g\\
C\%=\dfrac{0,2.136}{204,4}.100\%=13,3\%\)

a) Sửa đề: dd H2SO4 9,8%
Ta có: \(n_{H_2}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\) \(\Rightarrow m_{H_2}=0,35\cdot2=0,7\left(g\right)\)
Bảo toàn nguyên tố: \(n_{H_2SO_4}=n_{H_2}=0,35\left(mol\right)\) \(\Rightarrow m_{ddH_2SO_4}=\dfrac{0,35\cdot98}{9,8\%}=350\left(g\right)\)
\(\Rightarrow m_{dd}=m_{KL}+m_{H_2SO_4}-m_{H_2}=361,6\left(g\right)\)
b) Tương tự câu a
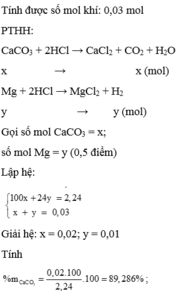
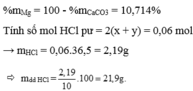
Zn + 2HCl → ZnCl2 + H2 (1)
Mg + 2HCl → MgCl2 + H2 (2)
\(n_{H_2}=\frac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PT1,2: \(\Sigma n_{HCl}=2\Sigma n_{H_2}=2\times0,3=0,6\left(mol\right)\)
\(\Rightarrow\Sigma m_{HCl}=0,6\times36,5=21,9\left(g\right)\)
\(\Rightarrow m_{ddHCl.14,6\%}=\frac{21,9}{14,6\%}=150\left(g\right)\)