Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn C
Gọi số mol của NO là a mol → số mol của N 2 O là 2a mol; số mol N 2 là 2a mol.
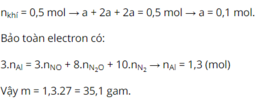

Có : nFe = nAl = nMg = 0,12 mol
Y : N2 ; N2O ; NO và NO2( N2 và NO2 có số mol bằng nhau)
=> Qui đổi : NO2 +N2 -> NO + N2O
=> Y trở thành : NO và N2O với số mol lần lượt là x và y.
Có : MY = 37g => mY = 37(x + y) = 30x + 44y
=> x = y(1)
Giả sử có z mol NH4NO3 trong muối
Bảo toàn e : 3nFe + 3nAl + 2nMg = 3nNO + 8nN2O + 8nNH4NO3
=> 3x + 8y + 8z = 0,96 mol(2)
Và : nHNO3 = (4x + 10y + 10z)
=> nH2O = ½ (nHNO3 – 4nNH4NO3) = (2x + 5y + 3z) mol
Bảo toàn khối lượng :
mY = mKL + mHNO3 – mH2O - mmuối X = (216x + 540y + 576z) – 62,52 = 37(x + y)
=> 179x + 503y + 576z = 62,52(3)
Từ (1),(2),(3) => x = y = 0,06 ; z = 0,0375 mol
=> nHNO3 pứ = 4x + 10y + 10z = 1,215 mol

nNO = 0,04 ; nN2O = 0,08 = nN2
n NO3- muối = n e = 3nNO +8n N2O + 10n N2
Bảo toàn nguyên tố N ta có:
nHNO3 ban đầu = n NO + 2n N2O + n NO3-/muối = 4nNO + 10nN2O + 12nN2 = 1,92 mol
⇒ V =1,92
Áp dụng định luật bảo toàn e có 3nAl = 3nNO + 8nN2O + 10nN2
⇒ nAl = 0,52 ⇒m = 14,04g
Đáp án A.

Muối sau pư gồm \(\left\{{}\begin{matrix}Fe\left(NO_3\right)_3:1\left(mol\right)\\Zn\left(NO_3\right)_2:0,6\left(mol\right)\end{matrix}\right.\)
Bảo toàn N: nHNO3 = 5,4 (mol)

QT cho e :
Al→ Al3++ 3e (1)
QT nhận e:
2NO3-+ 8e+ 10H+ → N2O + 5H2O (3)
0,24 0,3 ← 0,03 mol
NO3-+ 3e + 4H+→ NO+ 2H2O (4)
0,06 0,08← 0,02
Theo bán phản ứng (3) và (4) ta có:
nH+= 10.nN2O+ 4.nNO= 10.0,03 + 4.0,02= 0,38 mol≠ 0,58 mol
Do đó còn có thêm quá trình nhận e tạo NH4+
NO3-+ 8e + 10H+ → NH4+ + 3H2O (5)
0,16 ← 0,2
nH+ pt5= 0,58- 0,38= 0,2 mol
Theo bán phản ứng (3), (4), (5) ta có:
ne nhận= 8. nN2O+ 3.nNO+ 8/10.nH+= 0,24+ 0,06+ 0,16= 0,46 mol
Theo ĐL bảo toàn e : ne cho= ne nhận= 0,46 mol → nAl= 0,46/3 mol
→mAl= 4,14 gam
Đáp án D
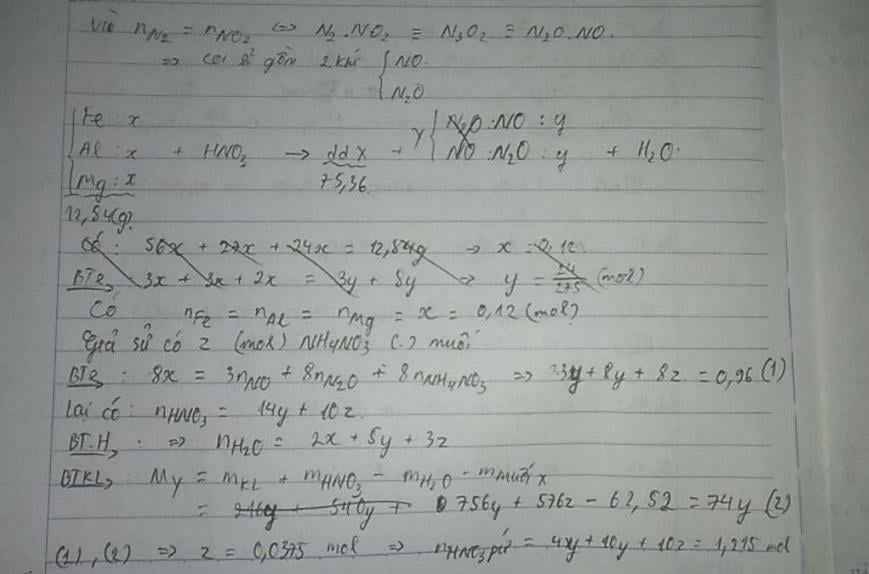
tỉ lệ là 46:6:9