Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Quy đổi A chỉ gồm Fe3O4 + CO → 19,2 gam (Fe : x mol + O : y mol) + CO2
19,2 gam (Fe : x mol + O : y mol) + HNO3 → Fe(NO3)3 + NO + H2O
Ta có hệ phương trình
(1) 56x + 16y = 19,2
(2) ĐLBT mol e : 3x = 2y + 0,1*3
→ x = 0,27 ; y = 0,255 → n(Fe3O4) = 0,09 mol → m1 = 20,880 gam
→ n(CO2) = n(CaCO3) = 0,09*4 – 0,255 = 0,105 → m2 = 20,685 gam
n(HNO3) = 0,27*3 + 0,1 = 0,91 mol
Khối lượng dung dịch tăng nên tạo BaCO3 (a) và Ba(HCO3)2 (b)
nBa(OH)2 = a + b = 0,06
Δm = 44(a + 2b) – 197a = 1,665
->a = 0,015 và b = 0,045
nCO2 = a + 2b = 0,105
X gồm nMgO = nFeO = nFe2O3 = nFe3O4 = x
-->Quy đổi Y thành Mg (x), Fe (6x) và O (9x – 0,105)
=>mY = 24x + 56.6x + 16(9x – 0,105) = 21
-> x = 0,045
->mX = 22,68
Bảo toàn electron: 2nMg + 3nFe = 2nO + 3nNO
nNO = 0,1
->V = 2,24 lít
=>nHNO3 = 4nNO + 2nO = 1

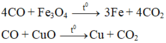
![]()
Khí thoát ra khỏi bình dẫn qua dung dịch Ca OH 2 thu được 5 gam kết tủa CaCO 3
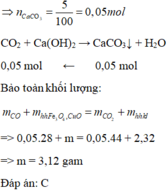

Pt:
Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O
0,1 → 0,4 0,1 0,1
Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4
0,1 ←0,1 → 0,1 0,2
Rắn B là 0,1 mol Cu → x = 6,4 (g)
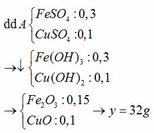



a) Gọi số mol của FeCO3: x (mol) ;
số mol của FeS2: y (mol)
4FeCO3 + O2 → Fe2O3 + 4CO2↑
x → 0,25x → x (mol)
4FeS2 +11O2 → 2Fe2O3 + 8SO2↑
y → 2,75y → 2y (mol)
∑ nO2 = 0,25x + 2,75y (mol)
Cùng điều kiện về nhiệt độ và áp suất nên tỉ lệ về thể tích = tỉ lệ về số mol
=> nN2 = 4nO2 = 4(0,25x + 2,75y)
=> nN2 = x + 11y (mol)
Vậy hỗn hợp Y gồm:

Khối lượng Fe có trong Z là:

Vì H = 80% => nFe2O3 (trong X) = 0,12. 100% : 80% = 0,15 (mol)
nFe2O3 dư (trong Z) = 0,15 – 0,12 = 0,03 (mol)
Khối lượng tạp chất trong Z = 27,96 – mFe – mFe2O3 dư = 27,96 – 0,24.56 – 0,03.160 = 9,72 (g)
Bảo toàn nguyên tố Fe => nFeCO3 + nFeS2 = 2nFe2O3(trong X)
=> x + y = 0,3 (2)
Từ (1) và (2) => x = 0,18 và y = 0,12 (mol)
Áp dụng công thức PV = nRT ( với n = nCO2 + nSO2 + nN2 = 0,18 + 2. 0,12 + 0,18 +11.0,12 = 1,92)
=> P.10 = 1,92.0,082. (136,5 +273)
=> P = 6,447 ( atm) ≈ 6,5 (atm)
Ta có: mA = mFeCO3 + mFeS2 + mtạp chất = 0,18.116 + 0,12.120 + 9,72 = 45 (g)
![]()
b) hỗn hợp Y gồm:

Cho hỗn hợp Y qua O2 ( xúc tác V2O5 ) có phản ứng sau:

Khối lượng dd sau: mdd sau = mSO3 + mH2O = 0,24. 80 + 592,8 = 612 (g)


\(n_{CO\left(bđ\right)}=\dfrac{5.6}{22.4}=0.25\left(mol\right)\)
\(CO+O_{oxit}\rightarrow CO_2\)
\(n_{CO}=n_Y=0.25\left(mol\right)\)
\(M_Y=18.8\cdot2=37.6\left(\dfrac{g}{mol}\right)\)
Bảo toàn khối lượng :
\(m_A=37.6\cdot0.25+12.32-0.25\cdot28=14.72\left(g\right)\)

a. Các phương trình có thể xảy ra:
C + O2 → t ∘ CO2 (1)
CaCO3 → t ∘ CaO + CO2 (2)
MgCO3 → t ∘ MgO + CO2 (3)
CuCO3 → t ∘ CuO + CO2 (4)
C +CO2 → t ∘ 2CO (5)
C + 2CuO → t ∘ 2Cu + CO2 (6)
CO + CuO → t ∘ Cu + CO2 (7)
CaO + 2HCl →CaCl2 + H2O (8)
MgO + 2HCl →MgCl2 + H2O (9)
CuO + 2HCl →CuCl2 + H2O (10)
b. Vì sau phản ứng có CO và CO2, các phản ứng xảy ra hoàn toàn nên các chất còn lại sau khi nung là CaO, MgO và Cu không có phản ứng (10)
mCu = 3,2(g) => mCuCO3 = 6,2g
Gọi số mol CaCO3, MgCO3, C trong hỗn hợp lần lượt là a, b, c.(*)
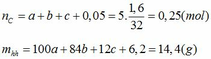
Giải ( *), (**), (***) ta được a=0,025; b=0,05; c=0,125.
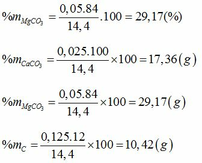

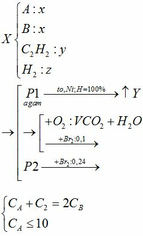
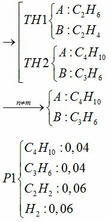
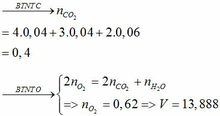
gọi số mol CO phảnứng là a mol suy ra số mol C02 tạo ra cũng là a mol
ta có (0,5-a)*28+44a=1.457*0,5*28 suy ra a=0,4 mol
suy ra số mol Fe304 là 0,1
m=23,2 gam
Mkhisp=28.1,457=40,796
=>sau phản ứng hỗn hợp khí gồm CO2; CO dư
do phản ứng xảy ra hoàn toàn,CO dư =>Fe3O4 hết chuyển thành Fe
PTHH 4CO+Fe3O4− − − (t∗) − − − >4CO2+3Fe
bđ:----0,5----------------------------------------(mol)
pứ:----x-----------x/4------------------x---------(mol)
sau:--(0,5-x)------x/4--------------------x----(mol)
áp dụng pp đưòng chéo ta có
\(\frac{nCO_2}{nCOdu}=\frac{4}{1}\\ hay:\frac{x}{0,5-x}=4\)
→ \(x=0,4\Rightarrow m=\left(0,\frac{4}{4}\right).232=23,2\left(g\right)\)
→ Đáp án D