

Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



+ Ở đây có 3 nguyên tố hoá học ở các ô số 5, 10, 11.
Nguyên tố ở ô số 10 là neon (Z = 10). Neon có 3 đồng vị là :
![]()
Tất cả 3 đồng vị của nguyên tố neon đều có cùng số electron là 10 (bằng số proton) nhưng số nơtron lần lượt là 10, 11, 12.
![]()
Đó là 2 đồng vị của nguyên tố bo (Z = 5)
Cả 2 đồng vị của nguyên tố bo đều có 5 electron nhưng số nơtron lần lượt là 5 và 6.
B 11 23
Đó là đồng vị của nguyên tố natri (Z = 11). Đồng vị này có 11 electron và 12 nơtron.

Đáp án A
Gọi tổng số proton và notron của phân tử X là p, n
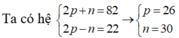
Gọi tổng số khối của A, B, C lần lượt là a, b, c
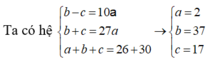
A có số khối là 2 → pA + nA = 2, mà pA, nA là các số nguyên dương → pA =1 (H)
B có số khối là 37 → pB + nB = 37
Luôn có pB ≤ nB ≤ 1,5 pB; 2pB ≤pB + nB = 37 ≤ 2,5pB
→ 14,8≤ pB ≤18,5 ,
→ pB = 15 (P), 16 (S), 17 (Cl)
C có số khối là 17 → pC + nC = 37
Luôn có pC ≤ nC ≤ 1,5 pC; 2pC ≤pC + nC = 17 ≤ 2,5pC
→ 6≤ pC ≤ 8,5
→ pC = 7 (N), 8 (O)
Để chất X có công thức ABC thì X có công thức là HClO.

Đáp án A
Gọi tổng số proton và notron của phân tử X là p, n
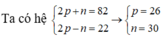
Gọi tổng số khối của A, B, C lần lượt là a, b, c
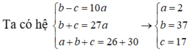
A có số khối là 2 → pA + nA = 2, mà pA, nA là các số nguyên dương
→ pA =1 (H)
B có số khối là 37 → pB + nB = 37
Luôn có pB ≤ nB ≤ 1,5 pB; 2pB ≤pB + nB = 37 ≤ 2,5pB
→ 14,8≤ pB ≤18,5 , → pB = 15 (P), 16 (S), 17 (Cl)
C có số khối là 17 → pC + nC = 37
Luôn có pC ≤ nC ≤ 1,5 pC; 2pC ≤pC + nC = 17 ≤ 2,5pC
→ 6≤ pC ≤ 8,5 → pC = 7 (N), 8 (O)
Để chất X có công thức ABC thì X có công thức là HClO.

Tổng số hạt cơ bản của nguyên tử nguyên tố X là 10. Số electron trong X là:
A. 3 B. 4. C. 6. D. 7
Ta có:
p<n<1,5p
3p<p+e+n<3,5p
3p<10<3,5p
=>p<3,3 và p>2,8
và p nguyên dương nên p=e=3
Vậy đáp án đúng là A

I trắc nghiệm
1.D
2.B
3.A
4.D
5.A
6.A
.IITự luận
1. NTK trung bình =\(\dfrac{12.98,89+13.1,11}{100}=12,0111\)
2.
20,18=\(\dfrac{20x+22\left(100-x\right)}{100}\) <=> x=91%(Ne 20)
Ne 22 là 100-91=9%