Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

câu A:
gọi hóa trị của Fe là x
\(\rightarrow Fe_2^xO_3^{II}\rightarrow x.2=II.3\rightarrow x=\dfrac{VI}{2}=III\)
vậy Fe hóa trị III
câu B:
gọi hóa trị của Zn là x
\(\rightarrow Zn_1^xCl^I_2\rightarrow x.1=I.2\rightarrow x=II\)
vậy Zn hóa trị II

1.\(a.CTHH:Fe_2\left(SO_4\right)_x\\ Tacó:56.2+\left(32+16.4\right).x=400\\ \Rightarrow x=3\\ VậyCTHH:Fe_2\left(SO_4\right)_3\\ b.CTHH:Fe_xO_3\\ Tacó:56.x+16.3=160\\ \Rightarrow x=2\\ VậyCTHH:Fe_2O_3\)
2. \(M_{Cu}=64\left(g/mol\right)\\ M_{H_2O}=2+16=18\left(g/mol\right)\\ M_{CO_2}=14+16.2=44\left(g/mol\right)\\ M_{CuO}=64+16=80\left(g/mol\right)\\ M_{HNO_3}=1+14+16.3=63\left(g/mol\right)\\ M_{CuSO_4}=64+32+16.4=160\left(g/mol\right)\\ M_{Al_2\left(SO_4\right)_3}=27.2+\left(32+16.4\right).3=342\left(g/mol\right)\)

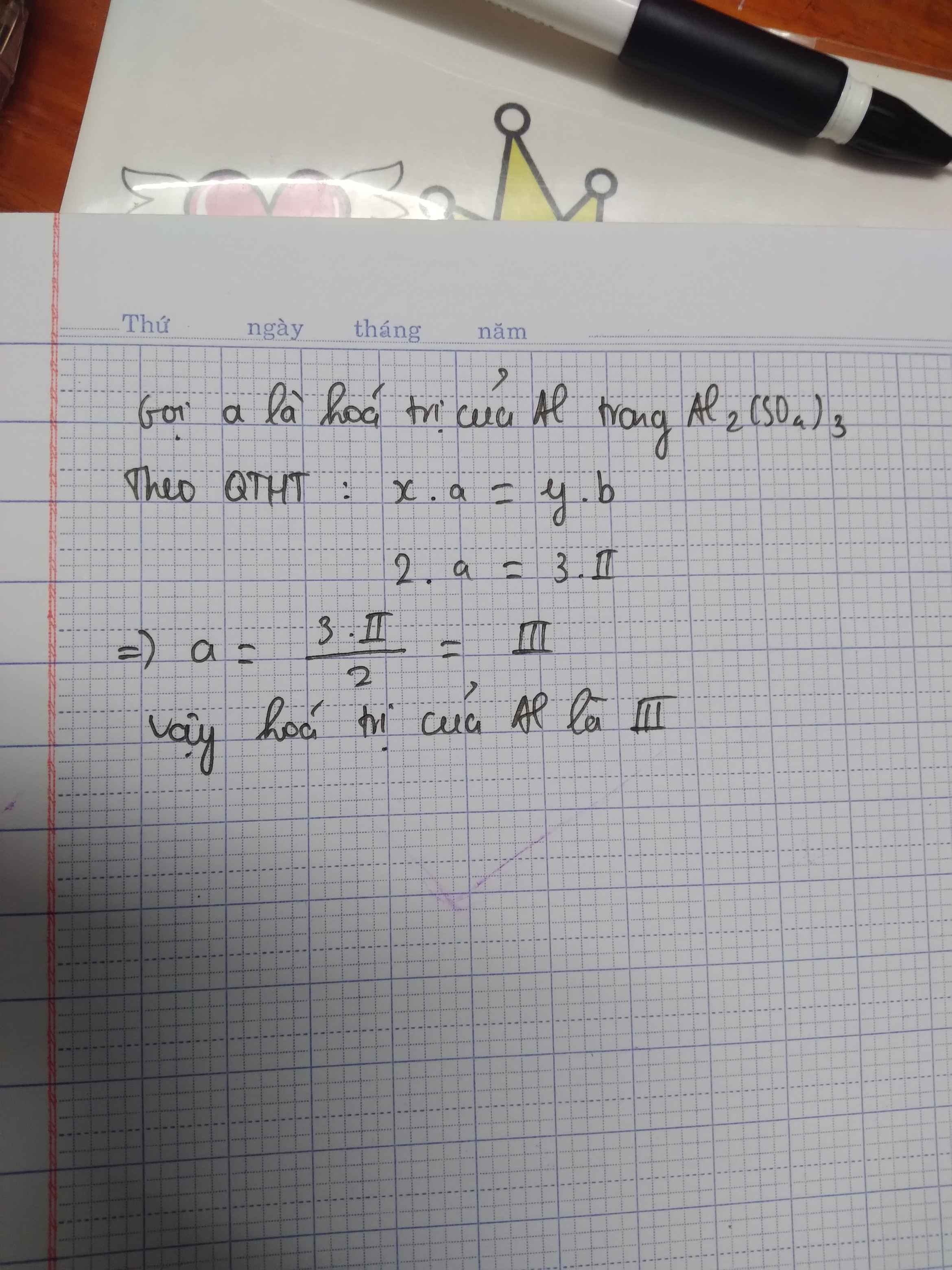 bài của em đây,chúc em học tốt nha ,tích cho chị vs luôn nhé
bài của em đây,chúc em học tốt nha ,tích cho chị vs luôn nhé

Ta có : \(n_C:n_S=2:1->\dfrac{1}{2}n_c=n_S\)
Lại có : \(m_C+m_S=5,6\)
-> \(n_C.12+n_S.32=5,6\)
=> \(n_C.12+\dfrac{1}{2}n_C.32=5,6\)
=> \(n_C=0,2\left(mol\right)\)
-> \(n_S=\dfrac{1}{2}.0,2=0,1\left(mol\right)\)
PTHH : \(C+O_2\underrightarrow{t^o}CO_2\) (1)
\(S+O_2\underrightarrow{t^o}SO_2\) (2)
Từ (1) -> \(n_C=n_{O_2}=0,2\left(mol\right)\)
-> \(V_{O_2\left(1\right)}=0,2.22,4=4,48\left(l\right)\)
Từ (2) -> \(n_S=n_{O_2}=0,1\left(mol\right)\)
\(V_{O_2\left(2\right)}=0,1.22,4=2,24\left(l\right)\)
=> \(V=\dfrac{V_{O_2\left(1\right)}+V_{O_2\left(2\right)}}{20\%}=33,6\left(l\right)\)

Về việc tính hoá trị là phải làm đặt hoá trị và giải, mình làm mẫu một bài nhé, bạn áp dụng cho tất cả các CTHH còn lại.
VD mình chưa biết hoá trị của Mg, Cl trong hợp chất MgCl2
Đặt: \(Mg^aCl^b_2\left(a,b:nguy\text{ê}n,d\text{ươ}ng\right)\\ QTHT:a.1=b.2\\ \Rightarrow\dfrac{a}{b}=\dfrac{2}{1}=\dfrac{II}{I}\\ \Rightarrow a=II;b=I\\ \Rightarrow Mg\left(II\right),Cl\left(I\right)\)
