Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Lời giải
n H C O O H = n C H 3 C O O H = 0 , 05 ( m o l ) ; n C 2 H 5 C O O H = 0 , 125 ( m o l ) ⇒ n a x i t < n a n c o l ⇒ b à i t o á n t í n h t h e o s ố m o l a x i t
=> Este gồm HCOOC2H5 và CH3COOC2H5 với n H C O O C 2 H 5 = n C H 3 C O O H = 80 % . 0 , 05 = 0 , 04 ( m o l ) V ậ y m e s t e = 6 , 48 ( g )
Đáp án B.

Ta có nC2H5OH = 5,75/46 = 0,125 mol. Đặt nHCOOH = nCH3COOH = x
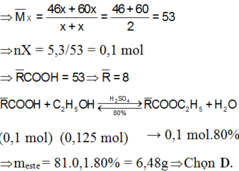

Đáp án A
n H C O O H = n C H 3 C O O H = 0 , 16 ( m o l ) ; n C H 3 O H = 0 . 08 ( m o l ) ; n C 2 H 5 O H = 0 . 12 ( m o l )
=>nếu H = 100% thì ancol hết, axit dư
=> bài toán tính theo ancol
H = 80%
=> nancol phản ứng = 0, 8.(0, 08 + 0,12) = 0,16 (mol) = naxit phản ứng
⇒ n H 2 O = 0 , 16 ( m o l ) ⇒ n a x i t p h ả n ứ n g = 1 2 n b a n đ ầ u ⇒ m a x i t p h ả n ứ n g = 1 2 16 , 96 = 8 , 48 ( g ) ⇒ n a n c o l p h ả n ứ n g = 0 , 8 . 8 , 08 = 6 , 464 ( g )
Bảo toàn khối lượng ta có:
meste = maxit phản ứng + mancol phản ứng - m H 2 O = 12,064(g)

Đáp án B
Hướng dẫn 2 axit có tỉ lệ mol 1:1 => Mtb= 53 => n(hỗn hợp 2 axit)= 5,3 /53= 0,1 mol
Vì số mol ancol lớn hơn số mol 2 axit nên ancol dư.
Số mol ancol pư = số mol 2 axit = 0,1 mol. áp dụng định luật bảo toàn khối lượng có
mancol + maxit = meste + mnước => 0,1.46 + 5,3 = meste + 0,1.18 => meste = 8,10 gam
H = 80% nên meste thu được = 8 , 10.80 100 = 6,48 gam.

Đáp án: D
Este tạo bởi ancol no đơn chức và axit no, đơn chức (tỷ lệ mol 1 : 1) nên este cũng no, đơn chức, có số mol bằng số mol ancol và axit (với hiệu suất 100%).
Đốt cháy este được nCO2 : nH2O
Áp dụng bảo toàn nguyên tố C có lượng CO2 thu được khi đốt cháy hỗn hợp A cũng tương đương lượng CO2 thu được khi đốt cháy este
=>nH2O = 0,8.0,1 = 0,08 mol => m = 1,44 gam

Chọn đáp án D
Đặt công thức trung bình cho hai axit là RCOOH
⇒ ![]()
Đặt công thức trung bình cho hai ancol là R’OH
![]()
có: ![]() mol;
mol;
![]() mol.
mol.
⇒ hiệu suất tính theo Y và este tạo thành là RCOOR’ có ![]() .
.
![]()

Giải thích: Đáp án A
Ta có số mol HCOOH và CH3COOH trong hỗn hợp X đều là 0,05 mol.
Ta có: ![]() nên ancol dư.
nên ancol dư.
Vậy hỗn hợp este gồm 0,04 mol HCOOC2H5 và 0,04 mol CH3COOC2H5 (do hiệu suất).
![]()

Đáp án: A
ta có: RCOOH + C2H5OH RCOOC2H5 + H2O
Ban đầu: 0,3----------------------0,25
Phản ứng: x<------------------------x <--------------------------------x
Sau pứ: 0,3 - x -----------------0,25-x
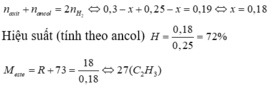

Đáp án C
Lượng este lớn nhất thu được là lượng este ở trạng thái cân bằng.
Khi đó: n H 2 O = 2 3 ( m o l ) ; n C H 3 C O O H = n C 2 H 5 O H = 1 3 ( m o l )
⇒ K C = 2 3 . 2 3 1 3 . 1 3 = 4
Để hiệu suất đạt 80% (tính theo axit) khi tỉến hành este hóa 1 mol CH3COOH thì neste = 0,8(mol)
G ọ i n C 2 H 5 O H b a n đ ầ u = x ( m o l )
=> Ở trạng thái cân bằng n C 2 H 5 O H = x - 0 , 8 ( m o l ) ; n C H 3 C O O H = 0 , 2 ( m o l ) ; n H 2 O = 0 , 8 ( m o l )
⇒ K C = 0 , 8 . 0 , 8 0 , 2 ( x - 0 , 8 ) = 4 ⇒ x = 1 , 6 ( m o l )