Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Thể tích khí H2: 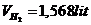

 Số mol
Số mol
Phương trình :



 khối lượng
khối lượng
Vậy khối lượng Mg : 
Vậy khối lượng Cu: 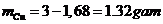

Số mol
Phương trình :

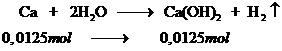
Số mol Ca(OH)2 tạo thành
Thể tích dd :
Nồng độ dd Ca(OH)2

nO2 = \(\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Pt: 2Cu + O2 \(\rightarrow\) 2CuO
x 0,5x x
3Fe + 2O2 \(\rightarrow\) Fe3O4
y 2/3y 1/3y
Theo bài ta có hpt:
\(\left\{{}\begin{matrix}64x+56y=23,2\\0,5x+\dfrac{2}{3}y=0,25\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}x=0,1\\y=0,3\end{matrix}\right.\)
mCuO = 0,1.80 = 8 g
mFe3O4 = 0,3.232 = 69,6g
=> %mCuO = \(\dfrac{8}{8+69,6}.100\%=10,3\%\)
%mFe3O4 = 100 - 10,3 = 89,7%

Zn+H2SO4->ZnSO4+H2
Fe+H2SO4->FeSO4+H2
gọi nZn là x->nH2SO4(1)=x(mol)
nFe là y->nH2SO4(2)=y(mol)
nH2SO4=1(mol)
Ta có:65x+56y=37.2
=>65x+65y<37.2
-> x+y< xấp xỉ 0.6(mol)
Mà theo đề bài,nH2SO4=1(mol)
->hỗn hợp tan hết,axit dư
Zn+H2SO4->ZnSO4+H2
Fe+H2SO4->FeSO4+H2
gọi nZn là x->nH2SO4(1)=x(mol)
nFe là y->nH2SO4(2)=y(mol)
nH2SO4=1(mol)
Ta có:65x+56y=37.2
=>65x+65y>37.2
-> x+y>xấp xỉ 0.6(mol)
56x+56y<37.2
->x+y<0.7
->0.6<x+y<0.7
mà nH2SO4 theo đề bài là 1mol
->hỗn hợp tan hết,axit dư ^^ xin lỗi bạn phần trước mình làm sai

\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: Ba + 2H2O --> Ba(OH)2 + H2
0,1<------------------------0,1
=> mBa = 0,1.137 = 13,7 (g)
=> mCu = 20 - 13,7 = 6,3 (g)
\(\left\{{}\begin{matrix}\%m_{Ba}=\dfrac{13,7}{20}.100\%=68,5\%\\\%m_{Cu}=\dfrac{6,3}{20}.100\%=31,5\%\end{matrix}\right.\)


Số mol
Phương trình
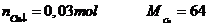
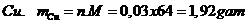
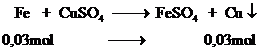
 khối lượng
khối lượng
Vậy khối lượng kim loại  là 1,92 gam
là 1,92 gam

Ta có pthh
2Al + 3H2SO4 \(\rightarrow\)Al2(SO4)3 + 3H2
Theo đề bài ta có
nAl=\(\dfrac{10,8}{27}=0,4mol\)
a, Theo pthh
nAl2(SO4)3 =\(\dfrac{1}{2}nAl=\dfrac{1}{2}.0,4=0,2mol\)
\(\Rightarrow\)mAl2(SO4)3=0,2.342=68,4 g
nH2=\(\dfrac{3}{2}nAl=\dfrac{3}{2}.0,4=0,6mol\)
\(\Rightarrow\)VH2=0,6.22,4=13,44 l
b, Khối lượng dd H2SO4 là
mddH2SO4 =\(\dfrac{mct.100\%}{C\%}=\dfrac{10,8.100\%}{10\%}=108g\)
Ta có: \(n_{Al}=\dfrac{10,8}{27}=0,4\left(mol\right)\)
PTHH: 2Al + 3H2SO4 (loãng) -> Al2(SO4)3 + 3H2
Theo PTHH và đề bài, ta có:
\(n_{H_2SO_4}=n_{H_2}=\dfrac{3.n_{Al}}{2}=\dfrac{3.0,4}{2}=0,6\left(mol\right)\)
\(n_{Al_2\left(SO_4\right)_3}=\dfrac{n_{Al}}{2}=\dfrac{0,4}{2}=0,2\left(mol\right)\)
a) Khối lượng muối tạo thành sau phản ứng:
\(m_{Al_2\left(SO_4\right)_3}=0,2.342=68,4\left(g\right)\)
Thể tích khí H2 thoát ra (đktc):
\(V_{H_2\left(đktc\right)}=0,6.22,4=13,44\left(l\right)\)
b) Khối lượng H2SO4:
\(m_{H_2SO_4}=0,6.98=58,8\left(g\right)\)
Khối lượng dung dịch H2SO4 đã dùng:
\(m_{ddH_2SO_4}=\dfrac{m_{H_2SO_4}.100\%}{C\%_{ddH_2SO_4}}=\dfrac{58,8.100}{10}=588\left(g\right)\)

\(n_{H_2}=\dfrac{0,56}{22,4}=0,025\left(mol\right)\)
\(PTHH:Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\uparrow\)
0,025 0,025
\(BaO+H_2O\rightarrow Ba\left(OH\right)_2\)
\(\rightarrow m_{Ba}=0,025.137=3,425\left(g\right)\\ \rightarrow\left\{{}\begin{matrix}\%m_{Ba}=\dfrac{3,425}{6,486}=52,81\%\\\%m_{BaO}=100\%-52,81\%=47,19\%\end{matrix}\right.\)


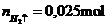

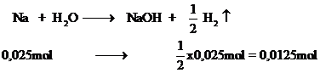
Bạn nên thêm ↑ vào sau chỗ \(H_2\) nhé
Cho Mg và Cu vào HCl thì chỉ có Mg pứ (Cu ko Pứ vì Cu đứng sau H trong dãy điện hóa)
Phương trình :



Vậy khối lượng Mg :
Vậy khối lượng Cu: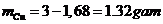
nH2=\(\dfrac{1,568}{22,4}=0,07\left(mol\right)\)
Mg+2HCl\(\rightarrow\)MgCl2+H2
0,07.........................0,07(mol)
Cu+HCl không pứ
\(\Rightarrow\)mMg=0,07.24=1,68(g)
\(\Rightarrow\)mCu=3-1,68=1,32(g)
Chúc bạn học tốt!