Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Xác định thành phần của hỗn hợp khí :
- Số mol CO 2 có trong hỗn hợp được tính theo (1) :
n CO 2 = n CaCO 3 = 1/100 = 0,01 mol
- Số mol CO có trong hỗn hợp được tính theo (2) :
n CO = n Cu = 0,64/64 = 0,01
Thành phần phần trăm theo thể tích của hỗn hợp khí được tính theo số mol của mỗi khí. Ta có kết quả : Hỗn hợp khí có 50% thể tích của mỗi khí.

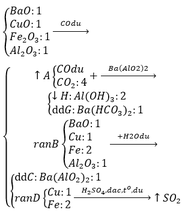
Các phương trình hoá học :
- CO 2 tác dụng với dung dịch Ca OH 2 dư, sinh ra kết tủa CaCO 3 :
CO 2 + Ca OH 2 → CaCO 3 ↓+ H 2 O (1)
- CO khử CuO thành kim loại Cu màu đỏ :
CO + CuO → CO 2 + Cu (2)

a) Khi đi vào dd Ca(OH)2 dư thì chỉ có CO2 phản ứng
CO2 + Ca(OH)2 --> CaCO3↓ + H2O
nCaCO3 = 1/100 = 0,01 mol = nCO2
Khi đi qua CuO dư đun nóng thì chỉ có CO phản ứng
CO + CuO --> CO2 + Cu
nCu = 0,64/64 = 0,01 mol = nCO
b) vậy hỗn hợp gồm CO và CO2 đều có số mol là 0,01 mol
=> % V mỗi khí = 50%
c) 2CO + O2 --> 2CO2
=> nO2 = \(\dfrac{nCO}{2}\)= 0,05 mol
=> Thể tích khí oxi cần dùng để đốt cháy hỗn hợp CO và CO2 là 0,05.22,4 = 1,12 lít.

CO2 + Ca(OH)2 → CaCO3↓ + H2O
0,34 ←0,34
CO + O(Oxit) → CO2
Nhận thấy:
nO = nCO2
mX = mO (oxit) + mY
=> mY = 37,68 – 16 . 0,34 = 32,24g


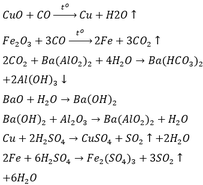


Tham khảo