Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Khi đi vào dd Ca(OH)2 dư thì chỉ có CO2 phản ứng
CO2 + Ca(OH)2 --> CaCO3↓ + H2O
nCaCO3 = 1/100 = 0,01 mol = nCO2
Khi đi qua CuO dư đun nóng thì chỉ có CO phản ứng
CO + CuO --> CO2 + Cu
nCu = 0,64/64 = 0,01 mol = nCO
b) vậy hỗn hợp gồm CO và CO2 đều có số mol là 0,01 mol
=> % V mỗi khí = 50%
c) 2CO + O2 --> 2CO2
=> nO2 = \(\dfrac{nCO}{2}\)= 0,05 mol
=> Thể tích khí oxi cần dùng để đốt cháy hỗn hợp CO và CO2 là 0,05.22,4 = 1,12 lít.

Xác định thành phần của hỗn hợp khí :
- Số mol CO 2 có trong hỗn hợp được tính theo (1) :
n CO 2 = n CaCO 3 = 1/100 = 0,01 mol
- Số mol CO có trong hỗn hợp được tính theo (2) :
n CO = n Cu = 0,64/64 = 0,01
Thành phần phần trăm theo thể tích của hỗn hợp khí được tính theo số mol của mỗi khí. Ta có kết quả : Hỗn hợp khí có 50% thể tích của mỗi khí.

\(n_{CaCO3}=\dfrac{2}{100}=0,02\left(mol\right)\)
Bảo toàn nguyên tố C: \(n_{CO}=n_{CaCO_3}=0,02\left(mol\right)\)
\(n_{Cu}=\dfrac{1,92}{64}=0,03\left(mol\right)\)
CuO + CO -------> Cu + CO2
0,02-------->0,02-->0,02
CuO + H2 -------> Cu + H2O
0,01<--------0,03-0,02=0,01
Phần trăm về thể tích cũng là phần trăm về số mol
=>\(\%V_{H_2}=\dfrac{0,01}{0,01+0,02}.100=33,33\%\)
=> %VCO=100- 33,33=66,67%
\(\%m_{H_2}=\dfrac{2.0,01}{2.0,01+44.0,02}.100=2,22\%\)
%mCO= 100-2,22=97,78%
b) \(V_{CO_2}=0,02.22,4=0,448\left(l\right)\)

1.
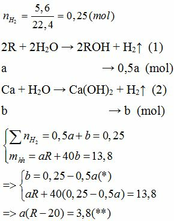
Vì b > 0, từ (*) => a < 0,25/0,5 = 0,5 thế vào (**)
=> R – 20 > 7,6
=> R > 27,6 (***)
Khi cho 8,58 gam R tác dụng với lượng dư HCl thì lượng H2 thoát ra lớn hơn 2,24 (lít)
2R + 2HCl → 2RCl + H2↑ (3)
Theo PTHH (3):
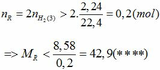
Từ (***) và (****) => 27, 6 < MR < 42,9
Vậy MR = 39 (K) thỏa mãn
2.
Ta có:
=> nKOH = nK = 0,2 (mol)
nCa(OH)2 = nCa = 0,15 (mol)
∑ nOH- = nKOH + 2nCa(OH)2 = 0,2 + 2.0,15 = 0,5 (mol)
Khi cho hỗn hợp Z ( N2, CO2) vào hỗn hợp Y chỉ có CO2 phản ứng
CO2 + OH- → HCO3- (3)
CO2 + 2OH- → CO32- + H2O (4)
CO32- + Ca2+ → CaCO3↓ (5)
nCaCO3 = 8,5/100 = 0,085 (mol) => nCO32-(5) = nCaCO3 = 0,085 (mol)
Ta thấy nCaCO3 < nCa2+ => phương trình (5) Ca2+ dư, CO32- phản ứng hết
TH1: CO2 tác dụng với OH- chỉ xảy ra phản ứng (4)
Theo (4) => nCO2 = nCO32-(4) = nCaCO3 = 0,085 (mol)
=> VCO2(đktc) = 0,085.22,4 = 1,904 (lít)
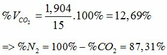
TH2: CO2 tác dụng với OH- xảy ra cả phương trình (3) và (4)
Theo (4): nCO2 = nCO32- = 0,085 (mol)
nOH- (4) = 2nCO32- = 2. 0,085 = 0,17 (mol)
=> nOH- (3)= ∑ nOH- - nOH-(4) = 0,5 – 0,17 = 0,33 (mol)
Theo PTHH (3): nCO2(3) = nOH- = 0,33 (mol)
=> ∑ nCO2(3+4) = 0,085 + 0,33 = 0,415 (mol)
=> VCO2 (ĐKTC) = 0,415.22,4 = 9,296 (lít)
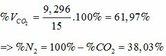

a, \(Na_2CO_3+2HCl\rightarrow2NaCl+CO_2+H_2O\)
\(K_2CO_3+2HCl\rightarrow2KCl+CO_2+H_2O\)
Ta có: 106nNa2CO3 + 138nK2CO3 = 43,5 (1)
Theo PT: \(n_{CO_2}=n_{Na_2CO_3}+n_{K_2CO_3}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Na_2CO_3}=0,15\left(mol\right)\\n_{K_2CO_3}=0,2\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Na_2CO_3}=\dfrac{0,15.106}{43,5}.100\%\approx36,55\%\\\%m_{K_2CO_3}\approx63,45\%\end{matrix}\right.\)
b, \(n_{HCl\left(pư\right)}=2n_{CO_2}=0,7\left(mol\right)\)
⇒ nHCl (dư) = 0,7.15% = 0,105 (mol)
\(\Rightarrow V_{ddHCl}=\dfrac{0,7+0,105}{2}=0,4025\left(M\right)\)
c, \(\left\{{}\begin{matrix}n_{NaCl}=2n_{Na_2CO_3}=0,3\left(mol\right)\\n_{KCl}=2n_{K_2CO_3}=0,4\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}C_{M_{NaCl}}=\dfrac{0,3}{0,4025}\approx0,745\left(M\right)\\C_{M_{KCl}}=\dfrac{0,4}{0,4025}\approx0,994\left(M\right)\end{matrix}\right.\)


