Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Điện phân dung dịch NaCl và HCl (điện cực trơ, màng ngăn xốp). Trong quá trình điện phân, so với dung dịch ban đầu thì giá trị pH của dung dịch thu được tăng lên. Lúc đầu dung dịch có pH nhỏ hơn 7, trong quá trình điện phân, HCl bị điện phân trước làm nồng độ H+ giảm nên pH bắt đầu tăng, khi H+ bị điện phân hết thì dung dịch có pH = 7. Tiếp đó NaCl bị điện phân làm cho nồng độ O H - tăng lên và pH tiếp tục tăng lên lớn hơn 7.
2 H C l → đ i ệ n p h â n d u n g d ị c h H 2 + C l 2 2 N a C l + H 2 O → c ó m à n g n g ă n x ố p đ i ệ n p h â n d u n g d ị c h 2 N a O H + H 2 ↑ + C l 2 ↑

Đáp án B
► Dung dịch thu được không pứ với AgNO₃
⇒ dung dịch thu được không còn Cl⁻
Ở đây ta cần chú ý, với H⁺ bị điện phân tại
catot và anot bị điện phân H₂O thì:
2H⁺ + 2e → H₂
2H₂O → 4H⁺ + O₂ + 4e
⇒ cộng lại cho khử e thì:
2H₂O → 2H₂ + O₂
⇒ xem như điện phân H₂O
⇒ pH không đổi
Mà ta thấy sau t(s) đầu tới t(s) sau
thì pH bị thay đổi
⇒ H₂O và H⁺ không bị điện phân
cùng lúc ngay t(s) đầu
► Mặt khác, phần xem như điện
phân H₂O không cần quan tâm
vì không có gì đặc biệt
⇒ xét phần còn lại thấy
nH⁺ giảm = nH⁺ bị điện phân
= 0,1 – 0,01 = 0,09 mol
nH⁺ sau khi điện phân
t(s) = 0,1 mol = nHCl ban đầu
⇒ nCl⁻ = 0,1 mol
BTe: nCu = (0,1 – 0,09) = 0,005 mol

ĐÁP ÁN A
pH = 13 > 7 => có OH-
, COH = 0,1M => nOH = 0,25 mol
Catot : 2H2O -> 2OH- + H2 – 2e
Anot : 2Cl- -> Cl2 + 2e
Bảo toàn e : nCl = nOH = 0,25 mol = nNaCl
=> %mNaCl đp = 62,5%
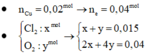
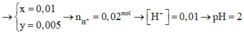
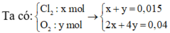
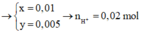

Chọn đáp án C.
Phương trình điện phân:
Dung dịch sau điện phân có môi trường axit, pH < 7