
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



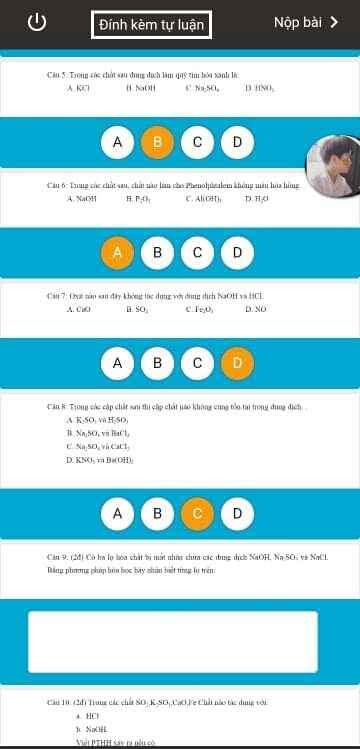
Câu 1 : B
Câu 2 : D
Câu 3 : C
Câu 4 : Cấu tạo nguyên tử :
+ Có 19 electron
+ Có 4 lớp electron
+ Có 1 electron lớp ngoài cùng
Câu 5 : B

Bài 5:
CTPT: CxHyO
\(n_{CaCO_3}=\dfrac{40}{100}=0,4\left(mol\right)\)
PTHH: 2CxHyO + \(\dfrac{4x+y-2}{2}\)O2 --to--> 2xCO2 + yH2O
\(\dfrac{0,4}{x}\)<--\(\dfrac{0,4\left(4x+y-2\right)}{4x}\)<------0,4
Ca(OH)2 + CO2 --> CaCO3 + H2O
0,4<-----0,4
=> \(M_{C_xH_yO}=\dfrac{7,4}{\dfrac{0,4}{x}}=18,5x\left(g/mol\right)\)
=> y + 16 = 6,5x (1)
Có \(n_{O_2}=\dfrac{19,2}{32}=0,6\left(mol\right)\)
=> \(\dfrac{0,4\left(4x+y-2\right)}{4x}=0,6\)
=> 0,8x = 0,4y - 0,8 (2)
(1)(2) => x = 4; y = 10
CTPT: C4H10O

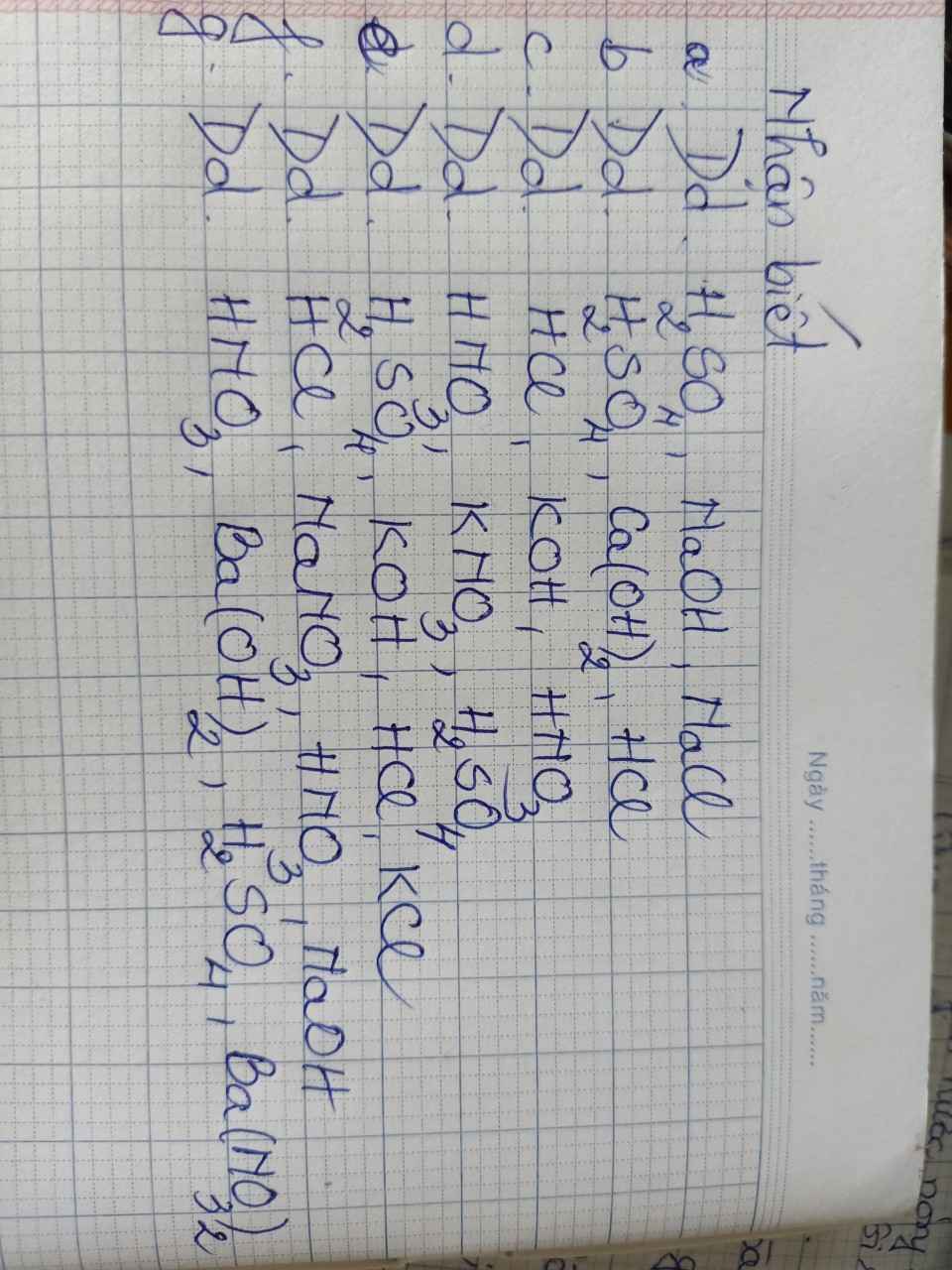
a) - Dùng quỳ tím:
+ Hóa đỏ -> dd H2SO4
+ Hóa xanh -> dd NaOH
+ Không đổi màu -> dd NaCl
b) - Dùng quỳ tím:
+ Hóa xanh -> dd Ca(OH)2
+ Hóa đỏ -> dd H2SO4, dd HCl
- Dùng dd BaCl2:
+ Có kết tủa trắng BaSO4 -> dd H2SO4
+ Không có kt trắng -> dd HCl
PTHH: H2SO4 + BaCl2 -> BaSO4 (kt trắng) + 2 HCl


a) nCuCl2 = 0,15.2 = 0,3 (mol)
PTHH: 2Al + 3CuCl2 --> 2AlCl3 + 3Cu
____0,2<------0,3--------->0,2---->0,3
=> m = 0,3.64 - 0,2.27 = 13,8 (g)
b) \(C_{M\left(AlCl_3\right)}=\dfrac{0,2}{0,15}=1,3333M\)


-
\(n_{CaCO_3}=\dfrac{15}{100}=0,15\left(mol\right)\)
\(Ca\left(HCO_3\right)_2=0,05.1=0,05\left(mol\right)\)
PTHH: Ca(OH)2 + CO2 --> CaCO3 + H2O
0,15<----0,15
Ca(OH)2 + 2CO2 --> Ca(HCO3)2
0,1<----------0,05
=> nCO2 = 0,25 (mol)
mtăng = mCO2 + mH2O - mCaCO3 = 3,2
=> 0,25.44 + 18.nH2O - 15 = 3,2
=> nH2O = 0,4 (mol)
Giả sử B là CxHy, A là CaHb
Theo giả thiết, có: \(\left\{{}\begin{matrix}n_{C_xH_y}=0,05\left(mol\right)\\n_{C_aH_b}=0,1\left(mol\right)\end{matrix}\right.\)
Bảo toàn C: 0,05x + 0,1a = 0,25
=> x + 2a = 5
Bảo toàn H: 0,05y + 0,1b = 0,8
=> y + 2b = 16
- TH1: x = 1; a = 2
Với x = 1 => y = 4 => b = 6
CTHH của A là C2H6, B là CH4 (TM)
- TH2: x = 3; a = 1
Với a = 1 => b = 4 => y = 8
CTHH của A là CH4, B là C3H8 (Loại)
Vậy CTHH của A là C2H6, B là CH4
-
+) Gọi \(\left\{{}\begin{matrix}n_{C_2H_6}=a\left(mol\right)\\n_{C_2H_4}=b\left(mol\right)\\n_{H_2}=c\left(mol\right)\end{matrix}\right.\)
=> \(a+b+c=0,5\) (1)
\(n_{H_2O}=\dfrac{18}{18}=1\left(mol\right)\)
Bảo toàn H: 6a + 4b + 2c = 2
=> 3a + 2b + c = 1 (2)
(1) => 2a + 2b + 2c = 1 (3)
(2) - (3) => a - c = 0 hay a = c
(1) => nY = 2a + b = 0,5
Mặt khác, mY = 30a + 28b + 2c = 32a + 28b (g)
Xét \(M_Y=\dfrac{m_Y}{n_Y}=\dfrac{32a+28b}{2a+b}=\dfrac{16\left(2a+b\right)+12b}{2a+b}=16+\dfrac{12b}{2a+b}\left(g/mol\right)>16\)
=> \(d_{Y/CH_4}>1\)
=> Y nặng hơn CH4
+) ngiảm = nH2 (pư) = \(\dfrac{11,2-8,96}{22,4}=0,1\left(mol\right)\)
Do Z không làm mất màu dd Br2
=> C2H4 phản ứng hết
nC2H4 = b = nH2(pư) = 0,1 (mol)
=> a = c = 0,2 (mol)
\(\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,1}{0,5}.100\%=20\%\\\%V_{C_2H_6}=\dfrac{0,2}{0,5}.100\%=40\%\\\%V_{H_2}=\dfrac{0,2}{0,5}.100\%=40\%\end{matrix}\right.\)









Bạn bấm lên máy giúp mk , mk không nhìn thấy