
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a)
- Cho các khí tác dụng với giấy quỳ tím ẩm
+ Ban đầu QT chuyển đỏ, sau đó mất màu: Cl2
\(Cl_2+H_2O⇌HCl+HClO\)
+ Không hiện tượng: O2, O3 (1)
- Dẫn khí ở (1) qua dd KI/hồ tinh bột:
+ Không hiện tượng: O2
+ dd chuyển màu xanh: O3
O3 + 2KI + H2O --> 2KOH + I2 + O2 (I2 làm xanh hồ tinh bột)
b)
- Cho các khí tác dụng với giấy quỳ tím ẩm:
+ QT chuyển đỏ: CO2
\(CO_2+H_2O⇌H_2CO_3\)
+ Không hiện tượng: O2, N2, O3 (1)
- Dẫn khí ở (1) qua dd KI/hồ tinh bột:
+ Không hiện tượng: O2, N2 (2)
+ dd chuyển màu xanh: O3
O3 + 2KI + H2O --> 2KOH + I2 + O2 (I2 làm xanh hồ tinh bột)
- Cho que đóm còn tàn đỏ tác dụng với khí ở (2):
+ Que đóm bùng cháy: O2
+ Que đóm tắt: N2
c)
- Dẫn các khí qua dd Br2 dư:
+ dd nhạt màu dần: SO2, H2S (1)
SO2 + Br2 + 2H2O --> H2SO4 + 2HBr
H2S + 4Br2 + 4H2O --> H2SO4 + 8HBr
+ Không hiện tượng: CO2
- Dẫn khí ở (1) qua dd Ca(OH)2
+ Kết tủa trắng: SO2
Ca(OH)2 + SO2 --> CaSO3 + H2O
+ Không hiện tượng: H2S

Câu 14:
a)
Bảo toàn H: \(n_{H_2SO_4\left(pư\right)}=n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Theo ĐLBTKL: mrắn trc pư + mH2SO4 = mrắn sau pư + mH2
=> m + 0,4.98 = 53,81 + 0,4.2
=> m = 15,41 (g)
b)
Gọi công thức chung của Al, Mg, Zn là R (hóa trị n), có số mol = a (mol)
Gọi số mol Fe là b (mol)
PTHH: 2R + nH2SO4 --> R2(SO4)n + nH2
a-------------------------->0,5an
Fe + H2SO4 --> FeSO4 + H2
b--------------------->b
=> 0,5an + b = 0,4 (1)
\(n_{SO_2}=\dfrac{10,304}{22,4}=0,46\left(mol\right)\)
PTHH: 2R + 2nH2SO4 --> R2(SO4)n + nSO2 + 2nH2O
a--------------------------->0,5an
2Fe + 6H2SO4 --> Fe2(SO4)3 + 3SO2 + 6H2O
b----------------------------->1,5b
=> 0,5an + 1,5b = 0,46 (2)
(1)(2) => b = 0,12 (mol)
=> \(\%Fe=\dfrac{0,12.56}{15,41}.100\%=43,61\%\)
Câu 15:
Gọi số mol Fe, O2(pư) là a, b (mol)
=> 56a + 32b = 8,64 (1)
\(n_{SO_2}=\dfrac{1,008}{22,4}=0,045\left(mol\right)\)
Fe0 - 3e --> Fe+3
a--->3a
O20 + 4e --> 2O-2
b--->4b
S+6 + 2e --> S+4
0,09<--0,045
Bảo toàn e: 3a - 4b = 0,09 (2)
(1)(2) => a = 0,117 (mol); b = 0,06526 (mol)
=> m = 0,117.56 = 6,552 (g)

a)
- Cho các dd tác dụng với dd HCl dư
+ Sủi bọt khí: Na2SO3
Na2SO3 + 2HCl --> 2NaCl + SO2 + H2O
+ Không hiện tượng: NaCl, Na2SO4, NaNO3 (1)
- Cho dd ở (1) tác dụng với dd BaCl2
+ Kết tủa trắng: Na2SO4
Na2SO4 + BaCl2 --> 2NaCl + BaSO4\(\downarrow\)
+ Không hiện tượng: NaCl, NaNO3 (2)
- Cho dd ở (2) tác dụng với dd AgNO3:
+ Không hiện tượng: NaNO3
+ Kết tủa trắng: NaCl
\(NaCl+AgNO_3\rightarrow NaNO_3+AgCl\downarrow\)
b)
- Cho các dd tác dụng với dd Ba(NO3)2
+ Không hiện tượng: HCl, HNO3 (1)
+ Kết tủa trắng: H2SO4(đ), H2SO4(l) (2)
- Cho dd ở (1) tác dụng với dd AgNO3:
+ Không hiện tượng: HNO3
+ Kết tủa trắng: HCl
\(AgNO_3+HCl\rightarrow AgCl\downarrow+HNO_3\)
- Cho Cu tác dụng với dd ở (2)
+ Không hiện tượng: H2SO4(l)
+ Chất rắn tan, dd có màu xanh: H2SO4(đ)
Cu + 2H2SO4 --> CuSO4 + SO2 + 2H2O
c)
- Cho các dd tác dụng với dd BaCl2
+ Không hiện tượng: NaOH
+ Kết tủa trắng: H2SO4, Fe2(SO4)3, CuSO4 (1)
\(BaCl_2+H_2SO_4\rightarrow BaSO_4\downarrow+2HCl\)
\(Fe_2\left(SO_4\right)_3+3BaCl_2\rightarrow2FeCl_3+3BaSO_4\downarrow\)
\(CuSO_4+BaCl_2\rightarrow BaSO_4\downarrow+CuCl_2\)
- Cho dd ở (1) tác dụng với dd NaOH
+ Không hiện tượng: H2SO4
2NaOH + H2SO4 --> Na2SO4 + 2H2O
+ Kết tủa nâu đỏ: Fe2(SO4)3
\(Fe_2\left(SO_4\right)_3+6NaOH\rightarrow2Fe\left(OH\right)_3\downarrow+3Na_2SO_4\)
+ Kết tủa xanh: CuSO4
\(CuSO_4+2NaOH\rightarrow Cu\left(OH\right)_2\downarrow+Na_2SO_4\)

Gọi số mol NaCl, NaBr là a, b (mol)
=> 58,5a + 103b = 52,9 (1)
Bảo toàn Cl: nAgCl = a (mol)
Bảo toàn br: nAgBr = b (mol)
=> 143,5a + 188b = 103,9 (2)
(1)(2) => a = 0,2 (mol); b = 0,4 (mol)
=> mNaCl = 0,2.58,5 = 11,7 (g)
=> nNaBr = 0,4.103 = 41,2 (g)



Câu 8:
Gọi số mol Na2CO3, CaCO3 là a, b (mol)
=> 106a + 100b = 15,6 (1)
PTHH: Na2CO3 + H2SO4 --> Na2SO4 + CO2 + H2O
a------------------------------>a
CaCO3 + H2SO4 --> CaSO4 + CO2 + H2O
b----------------------------->b
=> \(a+b=\dfrac{3,36}{22,4}=0,15\left(mol\right)\) (2)
(1)(2) => a = 0,1 (mol); b = 0,05 (mol)
=> mNa2CO3 = 0,1.106 = 10,6 (g); mCaCO3 = 0,05.100 = 5 (g)
Câu 9:
\(n_{H_2SO_4}=0,3.0,1=0,03\left(mol\right)\)
Bảo toàn H: nH2O = 0,03 (mol)
Theo ĐLBTKL: moxit + mH2SO4 = mmuối + mH2O
=> 2,81 + 0,03.98 = mmuối + 0,03.18
=> mmuối = 5,21 (g)

Bài 3:
- TH1: Chỉ tạo muối Na2SO3
\(n_{Na_2SO_3}=\dfrac{18,9}{126}=0,15\left(mol\right)\)
PTHH: 2NaOH + SO2 --> Na2SO3 + H2O
0,15<------0,15
=> V = 0,15.22,4 = 3,36 (l)
- TH2: Tạo muối Na2SO3, NaHSO3
nNaOH = 1.0,4 = 0,4 (mol)
PTHH: 2NaOH + SO2 --> Na2SO3 + H2O
0,4--->0,2------->0,2
Na2SO3 + SO2 + H2O --> 2NaHSO3
0,05----->0,05
=> nSO2 = 0,2 + 0,05 = 0,25 (mol)
=> V = 0,25.22,4 = 5,6 (l)
Bài 4:
\(n_{SO_2}=\dfrac{6,4}{64}=0,1\left(mol\right)\)
- Nếu chỉ tạo ra Na2SO3
\(n_{Na_2SO_3}=n_{SO_2}=0,1\left(mol\right)\Rightarrow m_{Na_2SO_3}=0,1.126=12,6\left(g\right)\)
- Nếu chỉ tạo ra NaHSO3
\(n_{NaHSO_3}=n_{SO_2}=0,1\left(mol\right)\Rightarrow m_{NaHSO_3}=0,1.104=10,4\left(g\right)\)
Do \(10,4< 11,5< 12,6\)
=> Tạo ra 2 muối Na2SO3, NaHSO3
Gọi \(\left\{{}\begin{matrix}n_{Na_2SO_3}=a\left(mol\right)\\n_{NaHSO_3}=b\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}a+b=0,1\\126a+104b=11,5\end{matrix}\right.\)
=> a = 0,05 (mol); b = 0,05 (mol)
=> nNaOH = 0,05.2 + 0,05 = 0,15 (mol)
=> \(V_{dd.NaOH}=\dfrac{0,15}{1}=0,15\left(l\right)\)








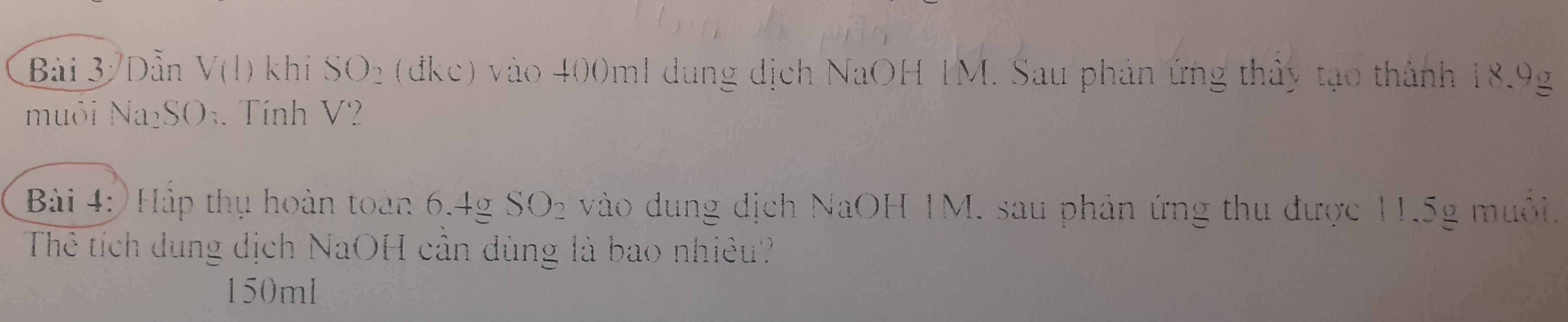

Câu 10:
\(n_{H_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
PTHH: Mg + H2SO4 --> MgSO4 + H2
0,05<--0,05<------------0,05
MgO + H2SO4 --> MgSO4 + H2O
0,15<--0,15
=> m = 0,05.24 + 0,15.40 = 7,2 (g)
Câu 11:
a) \(n_{Fe}=\dfrac{2,8}{56}=0,05\left(mol\right)\)
PTHH: 2Fe + 6H2SO4 --> Fe2(SO4)3 + 3SO2 + 6H2O
0,05-------------------------->0,075
=> VSO2 = 0,075.22,4 = 1,68 (l)
b) \(n_{Cu}=\dfrac{3,2}{64}=0,05\left(mol\right)\)
PTHH: Cu + 2H2SO4 --> CuSO4 + SO2 + 2H2O
0,05------------------------>0,05
=> VSO2 = 0,05.22,4 = 1,12 (l)