Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

+ Gọi V là thể tích của bình và p n là áp suất gây nổ.
+ Đối với khí nitơ ta có:
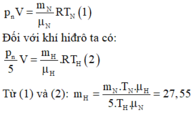

Trạng thái 1 là trạng thái khí ở điều kiện tiêu chuẩn: { V 1 = m p = 3 , 96 1 , 98 m 3 = 2 m 3 p 1 = p 0 = 1 a t T 1 = 0 0 C = 273 K
Trạng thái 2 là trạng thái khí ở điều kiện có thể nổ { V 2 = 0 , 04 m 3 p 2 = 60 a t T 2 = ?
Áp dụng công thức
p 1 V 1 T 1 = p 2 V 2 T 2 ⇒ T 2 = p 2 V 2 T 1 p 1 V 1 = 60.0 , 04.273 1.2 T 2 = 327 , 6 K
Mà T 2 = 273 + t 2 = 327 , 6 K ⇒ t 2 = 54 , 6 0 C

+ Trạng thái 1 là trạng thái khí ở điều kiện tiêu chuẩn:
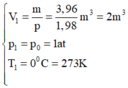
+ Trạng thái 2 là trạng thái khí ở điều kiện có thể nổ:


Do bình không dãn nở vì nhiệt, nên công do khí sinh ra : A' = p ∆ V = 0. Theo nguyên lí I, ta có :
∆ U = Q (1)
Nhiệt lượng do khí nhận được : Q = m c V ( T 2 - T 1 ) (2)
Mặt khác, do quá trình là đẳng tích nên :
![]()
Từ (2) tính được : Q = 15,58. 10 3 J.
Từ (1) suy ra: ∆ U = 15,58. 10 3 J.

Đáp án C
Gọi P o và T o lần lượt là áp suất và nhiệt độ ban đầu của khối khí trong bình
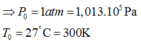
Gọi P và T lần lượt là áp suất và nhiệt độ của khối khí trong bình khi nút bắt đầu bị đẩy lên
![]()
Vì thể tích của khối khí là không thay đổi ngay trước khi nút bị đẩy lên, do đó theo định luật Sác – lơ, ta có:
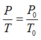

![]()
khi nút bắt đầu bị đẩy lên, ta có:
![]()

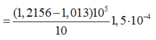
![]()

Đáp án D
Tới nhiệt độ nào thì van mở:
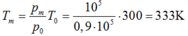
Bắt đầu từ nhiệt độ T m áp suất trong bình 1 tăng nhanh hơn trong bình 2,
nhưng khi hiệu áp suất vượt quá 105Pa thì van lại mở. Van giữ cho hiệu áp suất là 105Pa trong quá trình tăng nhiệt độ cho đến khi T = 500K. Khi đó:
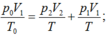
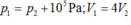
Ta có ![]() , từ đó rút ra
, từ đó rút ra ![]()

Gọi m1, m2 là khối lượng khí trong bình trước và sau khi nung nóng bình. Áp dụng phương trình Menđêlêep – Clapêrôn ta có:
p V = m 1 μ R T 1 , p V = m 2 μ R T 2 . ⇒ m 2 − m 1 = p V μ R ( 1 T 1 − 1 T 2 )
Với p = 50atm, V = 10 lít, μ = 2 g
R = 0 , 082 ( a t m . l / m o l . K ) Mà T 1 = 273 + 7 = 280 K ; T 2 = 273 + 17 = 290 K
⇒ m 2 − m 1 = 50.10.2 0 , 082 ( 1 280 − 1 290 ) m 2 - m 1 = 1 , 502 ( g )

Gọi m i , rrn là khối lượng khí trong bình trước và sau khi nung nóng bình.
Áp dụng phương trình Menđêlêep - Clapêrôn ta có:
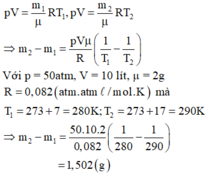
Gọi V là thể tích của bình và pn là áp suất gây nổ.
Đối với khí nitơ ta có: p n V = m N μ N R T N (1)
Đối với khí hiđrô ta có: p n 5 V = m H μ H R T H (2)
Từ (1) và (2) ⇒ m H = m N . T N . μ H 5. T H . μ N = 27 , 55 g